
Wetenschap
Hoe verhouden chemische vergelijkingen zich tot het behoud van massa?
De wet van behoud van massa
Het fundamentele principe in het spel is de wet van behoud van massa , die stelt dat het er niet in kan worden gecreëerd of vernietigd in een chemische reactie. Dit betekent dat de totale massa van de reactanten gelijk moet zijn aan de totale massa van de producten.
Balancing chemische vergelijkingen
* balanceren Een chemische vergelijking is cruciaal voor het aantonen van het behoud van massa. We passen de cijfers (coëfficiënten) aan voor de chemische formules om ervoor te zorgen dat hetzelfde aantal atomen van elk element zowel de reactant- als de productzijde verschijnt.
* Voorbeeld: De reactie van waterstofgas (H₂) met zuurstofgas (O₂) om water te vormen (H₂o) wordt weergegeven door de volgende onevenwichtige vergelijking:
H₂ + O₂ → H₂o
* Deze vergelijking is onevenwichtig omdat er 2 zuurstofatomen aan de reactantzijde zijn en slechts 1 aan de productzijde. Om het in evenwicht te brengen, voegen we een coëfficiënt van 2 toe voor h₂o:
2h₂ + o₂ → 2h₂o
* Nu is de vergelijking in evenwicht. We hebben 4 waterstofatomen en 2 zuurstofatomen aan beide zijden van de vergelijking.
Wat balanceren betekent
Het balanceren van een chemische vergelijking zorgt ervoor dat:
* Er gaan geen atomen verloren of gewonnen: Elk atoom dat aanwezig is in de reactanten moet ook aanwezig zijn in de producten.
* Mass is geconserveerd: Aangezien dezelfde atomen aanwezig zijn, moet de totale massa van de reactanten gelijk zijn aan de totale massa van de producten, waardoor de wet van het behoud van massa wordt gehandhaafd.
Belangrijke opmerking: Hoewel chemische vergelijkingen het behoud van massa aantonen, weerspiegelen ze niet altijd perfect real-world reacties. Factoren zoals energieveranderingen en de aanwezigheid van katalysatoren kunnen de exacte betrokken massa's beïnvloeden. Het principe van massabesparing blijft echter fundamenteel belangrijk bij het begrijpen van chemische reacties.
 Voorbeelden van secundaire verontreinigende stoffen
Voorbeelden van secundaire verontreinigende stoffen  Nieuw onderzoek biedt oplossing voor raadsel van koolstofopslag in de oceaan
Nieuw onderzoek biedt oplossing voor raadsel van koolstofopslag in de oceaan Miljoenen over Zuidoost zetten zich schrap voor mogelijke tornado's
Miljoenen over Zuidoost zetten zich schrap voor mogelijke tornado's Welke soort is het meest kwetsbaar voor menselijke invloeden?
Welke soort is het meest kwetsbaar voor menselijke invloeden?  Landvormen en natuurlijke rijkdommen van de kustvlakte
Landvormen en natuurlijke rijkdommen van de kustvlakte
Hoofdlijnen
- In de winkel gekochte kroontjeskruidplanten kunnen monarchrupsen blootstellen aan schadelijke pesticiden
- Genetisch gemodificeerd voedsel, wie moet het vertellen?
- Geometrie speelt een belangrijke rol in hoe cellen zich gedragen, onderzoekers rapporteren
- Wat is de wetenschappelijke classificatie van Linckia laevigata?
- Welke wetenschappen vormen milieuwetenschap?
- Kunnen condors terugkeren naar Noord-Californië?
- De hongerige insecten die de mestcrisis in Oeganda bestrijden
- Is een Liana een dier of plant?
- Wat is het belangrijkste product van fotosynthese dat in planten is opgeslagen?
- Ontwikkeling van een zeer duurzame enkel-atomige katalysator met behulp van industriële luchtbevochtiger

- Nieuwe biosensor stimuleert zweet terwijl de patiënt koel is en rust

- Onderzoekers ontwerpen dendrietvrije lithiumbatterij
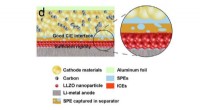
- Klaar voor de zomerzon met groene zonneschermen
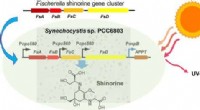
- Vloeibaar metaal bewezen goedkope en efficiënte CO2-converter
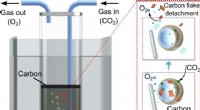
 Hoe kwantumfysici op zoek zijn naar leven op exoplaneten
Hoe kwantumfysici op zoek zijn naar leven op exoplaneten Waarom gaat elektriciteit naar de grond?
Waarom gaat elektriciteit naar de grond?  Beleggers straffen voor sociale onverantwoordelijkheid, afhankelijk van het percentage bedrijfsleiders met een diploma in de rechten
Beleggers straffen voor sociale onverantwoordelijkheid, afhankelijk van het percentage bedrijfsleiders met een diploma in de rechten Hoe je je draak kunt MRI:Onderzoekers ontwikkelen de eerste hersenatlas van baardagamen
Hoe je je draak kunt MRI:Onderzoekers ontwikkelen de eerste hersenatlas van baardagamen  Welke satelliet werd getroffen door een meteoriet?
Welke satelliet werd getroffen door een meteoriet?  Hoeveel centimeter zijn er in 39 meter?
Hoeveel centimeter zijn er in 39 meter?  Is het zonnestelsel een goed model voor elektronenstructuur?
Is het zonnestelsel een goed model voor elektronenstructuur?  Waarom is koolstof en geen ander element de basis van alle organische moleculen?
Waarom is koolstof en geen ander element de basis van alle organische moleculen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

