
Wetenschap
Wat is de reactievergelijking van waterstofsulfaat plus aluminiumhydroxide?
Hier is de evenwichtige chemische vergelijking:
3H₂SO₄ (aq) + 2al (oh) ₃ (s) → al₂ (So₄) ₃ (aq) + 6h₂o (l)
Hier is een uitsplitsing:
* reactanten:
* h₂so₄ (aq): Zwavelzuur, opgelost in water (waterig)
* AL (OH) ₃ (s): Aluminiumhydroxide, in vaste vorm
* Producten:
* al₂ (So₄) ₃ (aq): Aluminiumsulfaat, opgelost in water (waterig)
* h₂o (l): Water, in vloeibare vorm
Verklaring:
1. Neutralisatie van zure base: Zwavelzuur (H₂so₄) is een sterk zuur en aluminiumhydroxide (AL (OH) ₃ ₃) is een basis. Wanneer ze reageren, neutraliseren ze elkaar.
2. Zoutvorming: De waterstofionen (H⁺) van het zuur combineren met de hydroxide -ionen (OH⁻) van de basis om water te vormen (H₂o). De resterende ionen (aluminium en sulfaat) combineren om het zout, aluminiumsulfaat (al₂ (So₄) ₃) te vormen.
Laat het me weten als je nog andere chemische vragen hebt!
 Wetenschappers ontdekken het upcyclen van plastic om de uitstoot van broeikasgassen te verminderen
Wetenschappers ontdekken het upcyclen van plastic om de uitstoot van broeikasgassen te verminderen Koolzuurzuur kan water en koolstofdioxide vormen bij het verwarmen Hoeveel wordt er gevormd uit 6,20 g koolzuur?
Koolzuurzuur kan water en koolstofdioxide vormen bij het verwarmen Hoeveel wordt er gevormd uit 6,20 g koolzuur?  Hoeveel protonen in Lead-206?
Hoeveel protonen in Lead-206?  Is koper Turing Green een fysische of chemische verandering?
Is koper Turing Green een fysische of chemische verandering?  Waar komen de stoffen in oplossing oceanen vandaan?
Waar komen de stoffen in oplossing oceanen vandaan?
 Nieuw rapport schetst mogelijke opbrengstuitdagingen voor opschaling van natuurlijke landbouw zonder budget in India
Nieuw rapport schetst mogelijke opbrengstuitdagingen voor opschaling van natuurlijke landbouw zonder budget in India Golfstroom wervelt als bron van ijzer
Golfstroom wervelt als bron van ijzer Hoe een goedkope elektriciteitsmarkt Texas in de kou liet staan
Hoe een goedkope elektriciteitsmarkt Texas in de kou liet staan  EPA-chef:VS hebben één norm nodig voor brandstofefficiëntie
EPA-chef:VS hebben één norm nodig voor brandstofefficiëntie Afbeelding:Schoenmakerkrater, Australië
Afbeelding:Schoenmakerkrater, Australië
Hoofdlijnen
- De ziekte van Tay-Sachs is een menselijke genetische abnormaliteit die resulteert in cellen die zich ophopen en verstopt raken met zeer grote complexe lipiden welke cellulaire organel deze aandoening moet zijn?
- Wetenschappers ontdekken hoe een groep rupsen giftig werd
- Het verwarmen van eiwitten tot lichaamstemperatuur onthult nieuwe medicijndoelen
- Verwijderen welk organisme het voedselweb zal vernietigen?
- Kunnen veel populaties in een ecosysteem dezelfde niche delen?
- Hoe fotosynthese licht vangt en het leven op aarde aandrijft
- De vogels van een meedogenloos paradijs
- Wat zijn de 3 hoofdcellen in het immuunsysteem?
- Hoe vatten wetenschappers hun onderzoek samen?
- Materialen die opengaan in de hitte van het moment
- Spontaan patronen creëren in synthetische materialen

- Haaibestendig materiaal voor wetsuits kan levens helpen redden

- Nieuwe doelstelling voor ontwikkeling van innovatieve antibiotica
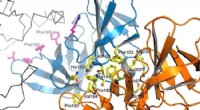
- Een manier om de absolute stereochemie van kleine, organische moleculen
 Astronomen onderzoeken radioburst-emissie van de magnetar XTE J1810−197
Astronomen onderzoeken radioburst-emissie van de magnetar XTE J1810−197 Laatste ijstijd:Neerslag veroorzaakte maximale opmars van Alpengletsjers
Laatste ijstijd:Neerslag veroorzaakte maximale opmars van Alpengletsjers Wanneer zowel zon als maan zichtbaar zijn, waarom is het verlichte gedeelte van niet in tweeën gedeeld door lijnaanvaarding
Wanneer zowel zon als maan zichtbaar zijn, waarom is het verlichte gedeelte van niet in tweeën gedeeld door lijnaanvaarding  Nieuw apparaat zoomt in op microbengedrag op de juiste schaal
Nieuw apparaat zoomt in op microbengedrag op de juiste schaal Een volledig elektrische magnetische logische poort
Een volledig elektrische magnetische logische poort China staat koppels derde kind toe tijdens demografische crisis
China staat koppels derde kind toe tijdens demografische crisis Waarin verschilt ammoniak van natriumhydroxide?
Waarin verschilt ammoniak van natriumhydroxide?  Wat is de werking van bijtende frisdrank op kleur fenolftalein?
Wat is de werking van bijtende frisdrank op kleur fenolftalein?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

