
Wetenschap
Koolzuurzuur kan water en koolstofdioxide vormen bij het verwarmen Hoeveel wordt er gevormd uit 6,20 g koolzuur?
1. Schrijf de gebalanceerde chemische vergelijking:
H₂co₃ (aq) → h₂o (l) + co₂ (g)
2. Bereken de molaire massa van koolzuur (H₂co₃):
* H:1.01 g/mol * 2 =2,02 g/mol
* C:12.01 g/mol
* O:16.00 g/mol * 3 =48,00 g/mol
* Totaal:2.02 + 12.01 + 48,00 =62,03 g/mol
3. Bereken de mol koolzuur:
* Mol =massa / molaire massa
* Mol =6,20 g / 62,03 g / mol =0,100 mol
4. Gebruik de molverhouding van de gebalanceerde vergelijking:
* De gebalanceerde vergelijking toont een 1:1 molverhouding tussen H₂co₃ en zowel H₂o als Co₂. Dit betekent dat voor elke 1 mol H₂co₃ je 1 mol h₂o en 1 mol co₂ krijgt.
5. Bereken de massa water (H₂o) en koolstofdioxide (CO₂):
* Molaire massa van H₂o: 18.02 g/mol
* Molaire massa van co₂: 44.01 g/mol
* massa van h₂o: 0,100 mol * 18,02 g/mol =1,80 g
* Mass van co₂: 0,100 mol * 44.01 g/mol =4,40 g
Antwoord:
* 6.20 g koolzuur vormt 1,80 g water en 4,40 g kooldioxide.
 Meer dan 20, 000 hectare van de oudste Oekraïense bossen worden natuurlijke monumenten
Meer dan 20, 000 hectare van de oudste Oekraïense bossen worden natuurlijke monumenten Leuke dingen om te doen in een gematigd loofbos
Leuke dingen om te doen in een gematigd loofbos Hoe veilig is de Hudson? Wetenschappers testen rivier, Adirondacks naar Ocean
Hoe veilig is de Hudson? Wetenschappers testen rivier, Adirondacks naar Ocean  Vingerafdruk voor de vorming van lachgasemissies
Vingerafdruk voor de vorming van lachgasemissies NASA-NOAA-satelliet vangt orkaan Barbara's oog dicht
NASA-NOAA-satelliet vangt orkaan Barbara's oog dicht
Hoofdlijnen
- Hoe ademen vogels beter? De ontdekking van onderzoekers zal je voor de gek houden
- Wat is de rol van logica in het dagelijks leven en wetenschapstechnologie PDF?
- Proteomics-onderzoek levert aanwijzingen op over de manier waarop tuberculose het immuunsysteem zou kunnen dwarsbomen
- Wat zijn vragen die wetenschappers kunnen beantwoorden?
- Welk phylum zijn orang -oetans?
- Bacterieel controlemechanisme voor aanpassing aan veranderende omstandigheden
- Experimentele evolutie:mariene roeipootkreeftjes kunnen zich genetisch aanpassen aan veranderende oceaanomstandigheden
- Kan de behandeling van hondendementie aanwijzingen opleveren voor de ziekte van Alzheimer bij mensen?
- Hoeveel allelen zijn er Mono Hybrid Cross betrokken?
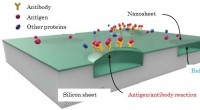
- Een halfgeleiderchip detecteert antigeenconcentraties bij 1 delen per quadriljoen molmassa
- Video:Hoe handontsmettingsmiddelen werken

- Nieuwe elektro-organische synthese maakt duurzame en groene productie van fijnchemicaliën mogelijk

- Smartphonelab levert testresultaten in een oogwenk

- Vormveranderend element vormt de sleutel tot antibacteriële coating

 Welke soorten bloemen bevinden zich in de toendra Biome?
Welke soorten bloemen bevinden zich in de toendra Biome?  Waar is de carno in fossiele jagers?
Waar is de carno in fossiele jagers?  Waarom gebruikt wetenschapper Robert Hazen drukbommen om mineralen op te blazen?
Waarom gebruikt wetenschapper Robert Hazen drukbommen om mineralen op te blazen?  Team ontwikkelt lichtsensor op nanoschaal die compatibel is met Etch-a-Sketch nano-elektronisch platform
Team ontwikkelt lichtsensor op nanoschaal die compatibel is met Etch-a-Sketch nano-elektronisch platform Wanneer begint de daglichtbesparingstijd in het VK 2011?
Wanneer begint de daglichtbesparingstijd in het VK 2011?  Onderzoekers overbruggen de kloof tussen disciplines om chemische reacties beter te begrijpen
Onderzoekers overbruggen de kloof tussen disciplines om chemische reacties beter te begrijpen Vleermuisvluchtmodel kan slimmer inspireren, wendbare drones
Vleermuisvluchtmodel kan slimmer inspireren, wendbare drones Welk experiment met betrokken kanonskogels?
Welk experiment met betrokken kanonskogels?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

