
Wetenschap
Waarom worden groep 2 metalen geclassificeerd als alkalische aardmetalen?
1. Alkalische oxiden:
* Wanneer deze metalen reageren met water, vormen ze hydroxiden die sterk alkalisch (basic) van aard zijn. Dit is waar de term "alkalisch" vandaan komt.
* Hun oxiden, gevormd door reactie met zuurstof, zijn ook alkalisch.
2. Aardachtige aard:
* De vroege alchemisten merkten op dat veel van deze metalen, zoals magnesium en calcium, van nature voorkomen in rotsen en mineralen, die zij 'aardes' noemden.
* Deze "aardse" aard draagt bij aan de naam "Alkalische aardmetalen."
3. Reactiviteit:
* Hoewel minder reactief dan de alkali -metalen (groep 1), zijn alkalische aardmetalen nog steeds behoorlijk reactief, vooral met water. Deze reactiviteit is te wijten aan hun twee valentie -elektronen, waardoor ze gemakkelijk bereid zijn om elektronen te doneren om ionische bindingen te vormen.
4. Eigenschappen:
* Deze metalen delen een gemeenschappelijke set eigenschappen, waaronder:
* Het zijn zilverwitte, glanzende metalen.
* Het zijn goede geleiders van warmte en elektriciteit.
* Ze hebben relatief lage dichtheden.
* Ze zijn moeilijker en sterker dan alkali metalen.
Samenvattend weerspiegelt de term "alkalische aardmetalen" de combinatie van hun alkalische oxiden, hun historische associatie met "aardes" en hun unieke chemische reactiviteit en fysische eigenschappen.
 Welke buiten planeet is voornamelijk gemaakt van ijs in plaats daarvan gas?
Welke buiten planeet is voornamelijk gemaakt van ijs in plaats daarvan gas?  Waarom wordt natriumsulfiet gebruikt om permanganaatvlekken te verwijderen?
Waarom wordt natriumsulfiet gebruikt om permanganaatvlekken te verwijderen?  Hoe verschilt de samenstelling van verschillende atomen?
Hoe verschilt de samenstelling van verschillende atomen?  Rioolschat:ingenieurs onthullen hoe ze processen kunnen optimaliseren voor het omzetten van zwavel in afvalwater in waardevolle materialen
Rioolschat:ingenieurs onthullen hoe ze processen kunnen optimaliseren voor het omzetten van zwavel in afvalwater in waardevolle materialen grafeen, perovskieten, en silicium - een ideale tandem voor efficiënte zonnecellen
grafeen, perovskieten, en silicium - een ideale tandem voor efficiënte zonnecellen
 Cristobal verzwakt tot tropische depressie als zware regenval Amerikaanse staten treft (update)
Cristobal verzwakt tot tropische depressie als zware regenval Amerikaanse staten treft (update) Typen door de mens veroorzaakte verontreinigende stoffen
Typen door de mens veroorzaakte verontreinigende stoffen  Regels voor het verwijderen van vleermuizen
Regels voor het verwijderen van vleermuizen Verbetering van klimaatmodellen om rekening te houden met plantgedrag levert goed nieuws op
Verbetering van klimaatmodellen om rekening te houden met plantgedrag levert goed nieuws op Wereld mist alle doelen om de natuur te redden, VN waarschuwt
Wereld mist alle doelen om de natuur te redden, VN waarschuwt
Hoofdlijnen
- Zenuwen controleren de bacteriële gemeenschap van het lichaam
- Boot die Steinbeck naar de Zee van Cortez bracht wordt gerestaureerd
- Waarom is het belangrijk dat een hypothese wordt gestart, dus kan worden gewijzigd?
- De menselijke huid was beter bestand tegen de zon voordat er zonneschermen en parasols waren. Een antropoloog legt uit waarom
- Hoe cilia worden georganiseerd:onderzoekers ontsluiten architectonische geheimen van ciliaire partities
- Wat is DNA -polymerase III?
- Je kunt echt op je naam lijken,
- Cellen verlaten de celcyclus wanneer ze?
- Wat doen de fasen in meiose?
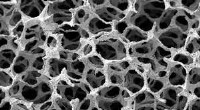
- Metaalschuim kan geluid onder hoge druk absorberen, omgevingen met hoge temperaturen zoals straalmotoren
- Een betere magere aardappelchips ontwerpen
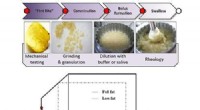
- Onderzoeksteam pioniert sneller, goedkopere en groenere manier om aminozuren te produceren uit plantaardig afval

- Biologen ontdekken carotenoïdenoverdracht tussen twee eiwitten

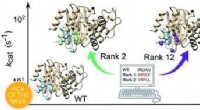
- Oude enzymen kunnen bijdragen aan groenere chemie
 Beheersen dieren het zuurstofgehalte van de aarde?
Beheersen dieren het zuurstofgehalte van de aarde? Het conflict in Oekraïne kan de graanprijzen op de lange termijn met 7% verhogen:studie
Het conflict in Oekraïne kan de graanprijzen op de lange termijn met 7% verhogen:studie  Wat is de rol van straling bij het verwarmen en koelen van de aarde?
Wat is de rol van straling bij het verwarmen en koelen van de aarde?  UITLEG:Wat zijn enkele belangrijke beslissingen bij het bestrijden van branden?
UITLEG:Wat zijn enkele belangrijke beslissingen bij het bestrijden van branden?  Waarom macrofagen rusten in gezond weefsel?
Waarom macrofagen rusten in gezond weefsel? TRAPPIST-1 is ouder dan ons zonnestelsel
TRAPPIST-1 is ouder dan ons zonnestelsel Wat het echt waard is om water naar huizen op het platteland van Zambia te leiden
Wat het echt waard is om water naar huizen op het platteland van Zambia te leiden Welke twee stoffen worden in kernreactoren als moderatoren gebruikt?
Welke twee stoffen worden in kernreactoren als moderatoren gebruikt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

