
Wetenschap
Waarom hebben alle istopes van een element dezelfde chemische mensen?
* Hetzelfde aantal protonen: Isotopen van een element hebben hetzelfde aantal protonen, dat het atoomnummer van het element en de identiteit ervan bepaalt. Dit betekent dat ze hetzelfde aantal elektronen hebben, die verantwoordelijk zijn voor chemische binding.
* Verschillende aantal neutronen: Isotopen verschillen in het aantal neutronen dat ze bevatten. Dit beïnvloedt hun massa, maar niet het aantal elektronen of protonen.
* Kleine verschillen in chemisch gedrag: De iets andere massa van isotopen kan leiden tot zeer subtiele verschillen in hun chemische reactiviteit, vooral in reacties met bindingstrillingen of diffusie. Deze verschillen zijn over het algemeen erg klein en vaak te verwaarlozen.
Waarom zijn de verschillen zo klein?
* Elektronen bepalen de reactiviteit: Chemisch gedrag wordt voornamelijk bepaald door het aantal en de opstelling van elektronen in een atoom, niet door het aantal neutronen. Omdat isotopen hetzelfde aantal elektronen hebben, hebben ze vergelijkbare elektronische configuraties en dus vergelijkbare chemische eigenschappen.
* massaverschillen zijn relatief klein: Het massaverschil tussen isotopen is meestal klein in vergelijking met de totale massa van het atoom. Dit betekent dat het verschil in hun gedrag ook erg klein is.
Voorbeeld:
Carbon-12 en koolstof-14 zijn beide isotopen van koolstof. Ze hebben hetzelfde aantal protonen (6) en elektronen (6), maar koolstof-14 heeft 8 neutronen in vergelijking met de 6 neutronen van Carbon-12. Dit maakt Carbon-14 iets zwaarder, maar het verandert niet significant zijn vermogen om bindingen met andere elementen te vormen.
Samenvattend:
Hoewel isotopen van een element hetzelfde aantal protonen en elektronen hebben, verschillen ze in het aantal neutronen. Dit verschil in massa kan leiden tot zeer subtiele variaties in hun chemische gedrag. Voor de meeste praktische doeleinden kunnen isotopen van een element echter worden beschouwd als dezelfde chemische eigenschappen.
 Wat zijn drie fysieke eigenschappen van het veranderen van in kleurbladeren?
Wat zijn drie fysieke eigenschappen van het veranderen van in kleurbladeren?  Stoffen hebben de neiging om volgens hun concentratiegradiënten te bewegen door het proces van?
Stoffen hebben de neiging om volgens hun concentratiegradiënten te bewegen door het proces van?  Protongeleiding regelen met licht
Protongeleiding regelen met licht Nieuw model maakt duidelijk waarom water bevriest bij verschillende temperaturen
Nieuw model maakt duidelijk waarom water bevriest bij verschillende temperaturen  Diamant uitrekken voor micro-elektronica van de volgende generatie
Diamant uitrekken voor micro-elektronica van de volgende generatie
 Hoe lang houden grijze beren overwinteren?
Hoe lang houden grijze beren overwinteren?  Fijnstofvervuiling:kunnen we microsensormetingen vertrouwen?
Fijnstofvervuiling:kunnen we microsensormetingen vertrouwen? Storm Dennis richt grote schade aan in het VK, delen van Frankrijk
Storm Dennis richt grote schade aan in het VK, delen van Frankrijk Pentagon-chef zegt dat klimaatverandering de veiligheid bedreigt:rapport
Pentagon-chef zegt dat klimaatverandering de veiligheid bedreigt:rapport Vervuiling door Britse auto's en bestelwagens kost £ 6 miljard per jaar in beschadigde gezondheid
Vervuiling door Britse auto's en bestelwagens kost £ 6 miljard per jaar in beschadigde gezondheid
Hoofdlijnen
- In bijensterfte, fungiciden komen naar voren als onwaarschijnlijke schurk
- Hoe wordt DNA gebruikt om organismen te helpen classificeren?
- Het leven is mooi voor de imkers in Griekenland, maar hoe lang?
- Hoe worden protista geclassificeerd?
- Wat doet een bladcel?
- Zeeleeuwen hebben unieke snorharen waarmee ze zelfs de snelste vis kunnen vangen
- Hoe DNA-profilering werkt
- De wetenschap van hoe planten trauma registreren omvat een voorloper van de calciumgolf
- Nieuwe studie heeft tot doel de redenen te begrijpen waarom genitale snijden bij vrouwen aanhoudt (update)
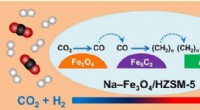
- Wetenschappers ontwikkelen efficiënte multifunctionele katalysator voor CO2-hydrogenering tot benzine
- Kleurveranderende vonken

- Onderzoekers rapporteren nieuwe klasse polyethyleenkatalysator

- Hiërarchisch 3D-printen van nanoporeus goud kan een revolutie teweegbrengen in het ontwerp van elektrochemische reactoren

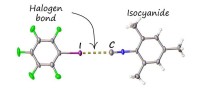
- Nieuwe niet-covalente binding blokkeert de afstotende geur van isocyaniden
 Wat is de term voor gassen die worden uitgevoerd door aerosolen en productie die de ozonlaag vernietigen?
Wat is de term voor gassen die worden uitgevoerd door aerosolen en productie die de ozonlaag vernietigen?  Planeetkannibalisme komt veel voor, zegt onderzoek naar kosmische tweelingen
Planeetkannibalisme komt veel voor, zegt onderzoek naar kosmische tweelingen  Wat is een regressielijn?
Wat is een regressielijn?  Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken
Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken Langzaam fietsen is niet alleen voor de lol - het is essentieel voor veel stadswerkers
Langzaam fietsen is niet alleen voor de lol - het is essentieel voor veel stadswerkers Een innovatieve methode voor het detecteren van in gebreke blijvende deelnemers op basis van schaarse reconstructie
Een innovatieve methode voor het detecteren van in gebreke blijvende deelnemers op basis van schaarse reconstructie Waarom zijn sommige sterrenbeelden zichtbaar naar de staat New York in april, maar niet in oktober?
Waarom zijn sommige sterrenbeelden zichtbaar naar de staat New York in april, maar niet in oktober?  Welke energieverandering vindt plaats als je een elektrisch licht aanzet?
Welke energieverandering vindt plaats als je een elektrisch licht aanzet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

