
Wetenschap
Welk van het oxide reageert met zowel zoutzuur als natriumhydroxide?
Dit is waarom:
* amfoterische oxiden kan zowel zuren als basen fungeren.
* met zuren , ze fungeren als bases en accepteren protonen (H+) om zouten en water te vormen.
* met bases , ze fungeren als zuren, doneren protonen (H+) om zouten en water te vormen.
Voorbeelden van amfoterische oxiden:
* aluminiumoxide (al₂o₃)
* zinkoxide (ZnO)
* lood (ii) oxide (PBO)
* tin (ii) oxide (sno)
reacties:
met zoutzuur:
* Al₂o₃ + 6Hcl → 2alcl₃ + 3h₂o
* ZnO + 2HCl → ZnCl₂ + H₂o
met natriumhydroxide:
* Al₂o₃ + 2naOH + 3H₂O → 2NA [AL (OH) ₄]
* ZnO + 2NaOH + H₂o → Na₂ [Zn (OH) ₄]
Belangrijke opmerking: Sommige oxiden, zoals die van overgangsmetalen, kunnen amfoterisch gedrag vertonen, afhankelijk van hun oxidatietoestand en reactieomstandigheden.
 Wat is de temperatuur van smeltpunt?
Wat is de temperatuur van smeltpunt?  Efficiënte synthese van meervoudig gesubstitueerde anilinen door domino-omlegging
Efficiënte synthese van meervoudig gesubstitueerde anilinen door domino-omlegging Hoe maak je een lab-on-a-chip helder en biocompatibel (met minder bloedspatten)
Hoe maak je een lab-on-a-chip helder en biocompatibel (met minder bloedspatten) Voedselwetenschappers upcyclen onverkocht brood tot smakelijke probiotische drank en verminderen voedselverspilling
Voedselwetenschappers upcyclen onverkocht brood tot smakelijke probiotische drank en verminderen voedselverspilling Is aardgas tastbaar of niet?
Is aardgas tastbaar of niet?
 Aanvaring met tanker heeft 400 ton olie gemorst voor de kust van China:autoriteiten
Aanvaring met tanker heeft 400 ton olie gemorst voor de kust van China:autoriteiten Voorbereidende werken starten omstreden Russische gaspijpleiding
Voorbereidende werken starten omstreden Russische gaspijpleiding Definitie van primaire consument
Definitie van primaire consument  De wetenschap van lentebloemen:hoe bloemblaadjes hun vorm krijgen
De wetenschap van lentebloemen:hoe bloemblaadjes hun vorm krijgen  Het complexe verband tussen bevolkingsafname en een opwarmende planeet
Het complexe verband tussen bevolkingsafname en een opwarmende planeet
Hoofdlijnen
- Wat is het enzym dat nodig is om ATP te maken?
- Welk hormoon produceert de pancrease?
- Wat is het belang van mesofylweefsel?
- Wat is de naam van uit dierlijke polysachariden samengestelde glucose-eenheden?
- Onderzoekers willen weten waarom beluga-walvissen nog niet zijn hersteld
- Welke factor heeft geen invloed op de enzymfunctie?
- Wat is de meeste takken van wetenschap?
- Wat betekent hypothese in de wetenschappelijke methode?
- Hoe verdeelt het cytoplasma zich tussen dochtercellen na mitose?
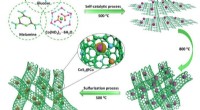
- S, N co-gedoteerde koolstof nanobuis ingekapselde CoS2@Co
- Video:Is het echt alleen chemisch reinigen?

- Polymerisatieproces van hydrogelmicrosferen op video

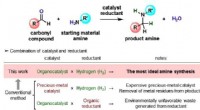
- Het naderen van een ideale aminozuursynthese met behulp van waterstof
- Zelfherstellend omgekeerd filter opent de deur voor veel nieuwe toepassingen

 Echte poolzwerven heeft mogelijk een ijstijd veroorzaakt
Echte poolzwerven heeft mogelijk een ijstijd veroorzaakt Hoe een coördinatienummer berekenen
Hoe een coördinatienummer berekenen  Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede
Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede Het benutten van symmetrieën:de computationele studie van solide oplossingen versnellen
Het benutten van symmetrieën:de computationele studie van solide oplossingen versnellen Onderzoeksnetwerk wil leerresultaten verbeteren voor leerlingen die ondervertegenwoordigd zijn in STEM
Onderzoeksnetwerk wil leerresultaten verbeteren voor leerlingen die ondervertegenwoordigd zijn in STEM Experiment zou voor het eerst de kwantumaard van grote massa's kunnen testen
Experiment zou voor het eerst de kwantumaard van grote massa's kunnen testen  Driedimensionale zelfassemblage met behulp van dipolaire interactie
Driedimensionale zelfassemblage met behulp van dipolaire interactie Uit onderzoek blijkt hoe koralen op hoge breedtegraden omgaan met de kou
Uit onderzoek blijkt hoe koralen op hoge breedtegraden omgaan met de kou
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

