
Wetenschap
Welke twee elementen ruilden Mendeleev in het periodiek systeem?
Dit is waarom:
* Atomische massa: Destijds regelde Mendeleev de elementen door de atoommassa te vergroten. Jodium had een iets lagere atoommassa dan tellurium, die jodium leek te plaatsen voor Tellurium.
* chemische eigenschappen: Mendeleev erkende echter dat de chemische eigenschappen van jodium meer vergelijkbaar waren met de halogenen (groep 17) dan op zuurstof en zwavel (groep 16), waar Tellurium behoorde.
Door hun positie te ruilen, zorgde Mendeleev ervoor dat elementen met vergelijkbare chemische eigenschappen werden gegroepeerd, waardoor zijn periodiek systeem nauwkeuriger werd.
Deze beslissing werd later gevalideerd wanneer het concept van atoomnummer werd geïntroduceerd, dat eigenlijk de positie van een element op het periodieke tabel definieert. Jodium heeft een hoger atoomnummer dan Tellurium, wat de intuïtie van Mendeleev bevestigt.
 Hoe de Ionische sterkte van een Solution
Hoe de Ionische sterkte van een Solution Wat zou er gebeuren met de entropie in reactie 203g 302g?
Wat zou er gebeuren met de entropie in reactie 203g 302g?  Wetenschappers onthullen rutheniumkatalysator voor het ontdekken en optimaliseren van nieuwe reacties
Wetenschappers onthullen rutheniumkatalysator voor het ontdekken en optimaliseren van nieuwe reacties  Bananenschillen maken suikerkoekjes beter voor je
Bananenschillen maken suikerkoekjes beter voor je Een verbeterde veiligheidsnorm voor bionische apparaten
Een verbeterde veiligheidsnorm voor bionische apparaten
 Wat gebeurt er als je half lucht en half helium in een ballon stopt?
Wat gebeurt er als je half lucht en half helium in een ballon stopt?  Fluisterende dennen:Bomen vertellen het verhaal van het slagschip uit de Tweede Wereldoorlog
Fluisterende dennen:Bomen vertellen het verhaal van het slagschip uit de Tweede Wereldoorlog Soorten Eetbare Paddenstoelen in Texas
Soorten Eetbare Paddenstoelen in Texas 7 Classificaties van Earthworms
7 Classificaties van Earthworms Is het waarschijnlijker dat op technologie gebaseerde intelligentie zich op het land of in het water zal ontwikkelen?
Is het waarschijnlijker dat op technologie gebaseerde intelligentie zich op het land of in het water zal ontwikkelen?
Hoofdlijnen
- Waarom het laten ontsnappen van zalm gunstig zou kunnen zijn voor beren en vissers
- Gewonde zeeschildpad genezen met 3D-printen
- Wetenschapper van Harvard zegt dat wij eten en koken
- Wetenschappers leggen uit hoe chromosomen zich reorganiseren na celdeling
- Wat zijn twee functies van het cytoskelet in dierlijke cellen?
- Wetenschappers tonen aan dat eiwitten die cruciaal zijn in dag-nachtcycli cellen ook beschermen tegen mutaties
- Hoe worden massa's zenuwweefsel genoemd?
- Welke materialen kan ik gebruiken om een DNA-model te maken?
- Hersendood hoe werkt
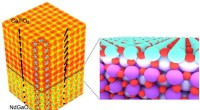
- Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen
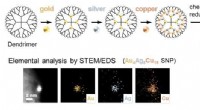
- Sub-nanodeeltjeskatalysatoren gemaakt van muntelementen als effectieve katalysatoren
- Middelbare scholieren ontwikkelen een goedkoop filter om lood uit kraanwater te verwijderen

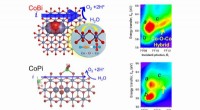
- Wetenschappers richten zich op röntgenstraling om nieuwe brandstofkatalysator te ontdekken
- Een topjaar voor farma

 Overstromingsrisico voor woningen met lage inkomens in de VS zou tegen 2050 kunnen verdrievoudigen
Overstromingsrisico voor woningen met lage inkomens in de VS zou tegen 2050 kunnen verdrievoudigen Hoe ontstaat solistion?
Hoe ontstaat solistion?  Holografisch kosmologisch model en thermodynamica aan de horizon van het heelal
Holografisch kosmologisch model en thermodynamica aan de horizon van het heelal Kun je echt een explosie ontlopen?
Kun je echt een explosie ontlopen?  Welke gesteenten worden onder water gevormd?
Welke gesteenten worden onder water gevormd?  Wat is het aantal kg in 245 pond?
Wat is het aantal kg in 245 pond?  Wat gebeurt er als ijzer- en kopersulfaat reageren?
Wat gebeurt er als ijzer- en kopersulfaat reageren?  Wat zijn de essentiële organen van het mannelijke reproductieve systeem?
Wat zijn de essentiële organen van het mannelijke reproductieve systeem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

