
Wetenschap
Waarom heeft ammoniak een ongewoon hoog kookpunt?
Hier is een uitsplitsing:
* waterstofbinding: Ammoniakmoleculen hebben een zeer polaire N-H-binding. Het stikstofatoom is meer elektronegatief dan waterstof, waardoor een gedeeltelijke negatieve lading op de stikstof en een gedeeltelijke positieve lading op de waterstof ontstaat. Deze gedeeltelijke ladingen zorgen voor sterke dipool-dipool interacties, met name waterstofbinding . Waterstofbinding is een bijzonder sterk type intermoleculaire kracht.
* klein formaat: Ammoniak is een klein molecuul, waardoor de waterstofbindingen vrij dicht bij elkaar en sterk kunnen zijn.
* Andere factoren: Hoewel waterstofbinding de primaire bijdrage levert, spelen andere factoren zoals Van der Waals -krachten ook een rol in het kookpunt van ammoniak.
Vergelijking:
Overweeg methaan (ch₄). Het heeft een vergelijkbaar molecuulgewicht als ammoniak maar mist waterstofbinding. Methaan heeft alleen zwakke Van der Waals-krachten die zijn moleculen bij elkaar houden, wat resulteert in een veel lager kookpunt (-161,5 ° C) vergeleken met ammoniak (-33,34 ° C).
Samenvattend: Het ongewoon hoge kookpunt van ammoniak is voornamelijk te wijten aan de sterke waterstofbinding tussen zijn moleculen. Deze sterke intermoleculaire kracht vereist meer energie om te overwinnen, wat resulteert in een hoger kookpunt.
 Olie-industrie onder druk om te reageren op klimaatverandering
Olie-industrie onder druk om te reageren op klimaatverandering Algenbloei in het centrale bassin van Lake Eries kan neurotoxines produceren
Algenbloei in het centrale bassin van Lake Eries kan neurotoxines produceren Om kusteigendom te redden van stijgende zeeën, we hebben gezamenlijke planning nodig
Om kusteigendom te redden van stijgende zeeën, we hebben gezamenlijke planning nodig Extreme droogte duwt deel van Utahs Great Salt Lake naar laagste niveau
Extreme droogte duwt deel van Utahs Great Salt Lake naar laagste niveau Permafrost in continue beweging
Permafrost in continue beweging
Hoofdlijnen
- Hoe vindt een mug menselijk lichaam?
- Vertrouwen op GPS voorkomt dat delen van uw hersenen worden geactiveerd
- Wat is bacteriële spore?
- Welke term hoort niet thuis in dit productcollageencelmatrixproduct?
- Hoeveel DNA kan bij een mens worden gevonden?
- Vrouwelijke dikhoornschapen met kleinere horens zijn minder geschikt voor de voortplanting, zo blijkt uit onderzoek
- Cellen van een groep herschikken?
- Hoe brengt het gezin cultuur over?
- Als talen botsen, wie overleeft er dan?
- Veilig printen met onzichtbare inkt op waterbasis

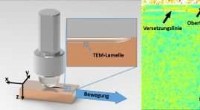
- Materiaalonderzoekers bestuderen de oorzaken van slijtage - permanente moleculaire modificaties treden op bij het eerste contact
- Machine-learningsysteem versnelt ontdekking van nieuwe materialen voor 3D-printen

- Studie zet vraagtekens bij de rol van loodvergiftiging bij sterfgevallen door Franklin Expedition

- Onderzoekers onthullen moleculaire basis van visie

 Hoeveel water en zonlicht heeft een plant nodig?
Hoeveel water en zonlicht heeft een plant nodig?  Opstand aan de horizon? Hoe jongeren echt over digitale technologie denken
Opstand aan de horizon? Hoe jongeren echt over digitale technologie denken Inzoomen op het landschap van Mexico
Inzoomen op het landschap van Mexico Welke twee klassen materialen zullen in water oplossen?
Welke twee klassen materialen zullen in water oplossen?  Verloren continenten gevonden diep onder de grond zo oud als de aarde werpen licht op de vorming van planeten
Verloren continenten gevonden diep onder de grond zo oud als de aarde werpen licht op de vorming van planeten Wat is experiment?
Wat is experiment?  Nieuwe faciliteit om omstandigheden op Venus te simuleren
Nieuwe faciliteit om omstandigheden op Venus te simuleren Nieuwe theorie beweert de zwaartekracht van Einstein te verenigen met de kwantummechanica
Nieuwe theorie beweert de zwaartekracht van Einstein te verenigen met de kwantummechanica
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

