
Wetenschap
Welk element zou reactiever zijn dan magnesium?
* Inzicht in reactiviteit: De reactiviteit in metalen neemt in het algemeen toe naarmate u naar beneden en naar links op het periodiek systeem gaat. Dit komt omdat:
* elektronegativiteit: Metalen aan de linkerkant van het periodiek systeem hebben een lagere elektronegativiteit, wat betekent dat ze gemakkelijk elektronen verliezen om positieve ionen te vormen.
* ionisatie -energie: Metalen die de tafel liggen, hebben lagere ionisatie -energieën, waardoor het gemakkelijker is om elektronen te verwijderen.
* Positie van Magnesium: Magnesium bevindt zich in groep 2 (alkalische aardmetalen) van het periodiek systeem.
* Meer reactieve elementen: Elementen die * meer * reactief zijn dan magnesium zouden worden gevonden:
* links: Elementen zoals natrium (NA) en kalium (k) zijn reactiever.
* hieronder: Elementen zoals calcium (CA), strontium (SR) en barium (BA) zijn meer reactief.
Daarom zijn elementen zoals natrium, kalium, calcium, strontium en barium allemaal reactiever dan magnesium.
 Onderzoekers gebruiken drukgevoelige moleculaire materialen om koeltechnologie te benutten
Onderzoekers gebruiken drukgevoelige moleculaire materialen om koeltechnologie te benutten Wat zijn verbindingen die de oppervlaktespanning van water verlagen?
Wat zijn verbindingen die de oppervlaktespanning van water verlagen?  Hoeveel atomen zitten er in Pbl2?
Hoeveel atomen zitten er in Pbl2?  Skeletstructuur van de elementen van het periodiek systeem?
Skeletstructuur van de elementen van het periodiek systeem?  Hoe kan de brekingsindex voor verschillende stoffen wiskundig worden bepaald?
Hoe kan de brekingsindex voor verschillende stoffen wiskundig worden bepaald?
 Nieuw ontdekte zoute subglaciale meren kunnen helpen bij het zoeken naar leven in het zonnestelsel
Nieuw ontdekte zoute subglaciale meren kunnen helpen bij het zoeken naar leven in het zonnestelsel Nog meer geëvacueerd nu vroege bosbranden West-Canada teisteren
Nog meer geëvacueerd nu vroege bosbranden West-Canada teisteren  Afbeelding:Golf van Kutch, India
Afbeelding:Golf van Kutch, India Record droogte grijpt Duitse graanschuur in de greep
Record droogte grijpt Duitse graanschuur in de greep Waarom het economisch gezien niet zinvol is om de klimaatverandering te negeren bij ons herstel van de pandemie
Waarom het economisch gezien niet zinvol is om de klimaatverandering te negeren bij ons herstel van de pandemie
Hoofdlijnen
- Wat is een wetenschappelijke sleutel?
- Hoe is de vorm van amylase gerelateerd aan zijn functie?
- Zijn planten die Cross Pollinate Called Offspring?
- Zoektocht naar nieuwe medicijnen kan worden geholpen door celontdekking
- Welke wetenschapper ontwikkelde theorieën over evolutie?
- Welke cellen kunnen worden gezien door het menselijk oog?
- Gemeenschappelijk element in nucleïnezuren en eiwitstructuur?
- Zeldzame fossiele tanden vernietigen lang gekoesterde opvattingen over de evolutie van gewervelde dieren
- Hoe vissen aan hun stekels kwamen
- Destabilisatieprocessen in schuim

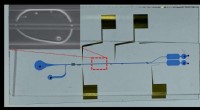
- Microfluïdisch systeem met celscheidende krachten kan ontrafelen hoe nieuwe pathogenen aanvallen
- Bioplottering van bot-mimetische 3D-weefselsteigers met osteogene effecten

- Nieuw ontwikkelde COVID-19-test detecteert en identificeert specifieke varianten met 100% nauwkeurigheid
- Enorm potentieel voor elektronisch textiel gemaakt met nieuwe cellulosedraad

 Buigbare opto-elektronische apparaten mogelijk maken:Galliumnitride-microstaafjes gekweekt op grafeensubstraten
Buigbare opto-elektronische apparaten mogelijk maken:Galliumnitride-microstaafjes gekweekt op grafeensubstraten Tijdreizen naar de toekomst is volledig mogelijk
Tijdreizen naar de toekomst is volledig mogelijk Het deel van een atoom dat zich buiten de kern bevindt is _______.?
Het deel van een atoom dat zich buiten de kern bevindt is _______.?  Onderzoekers bereiken een efficiënte afgifte van voedingsstoffen aan de bladeren van gewassen door middel van oppervlakteruwheidstechniek van nanomaterialen
Onderzoekers bereiken een efficiënte afgifte van voedingsstoffen aan de bladeren van gewassen door middel van oppervlakteruwheidstechniek van nanomaterialen  Hoe weeft een spin zijn web?
Hoe weeft een spin zijn web? SpaceX lanceert raket vanaf NASA's historische maanpad
SpaceX lanceert raket vanaf NASA's historische maanpad Hoe steden in het Westen water hebben te midden van droogte
Hoe steden in het Westen water hebben te midden van droogte  Nieuw microscoopconcept kan de stralingsdosis duizendvoudig verminderen
Nieuw microscoopconcept kan de stralingsdosis duizendvoudig verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

