
Wetenschap
Welk element reageert met H2O om H2 te produceren?
Dit is waarom:
* Alkali metalen zijn zeer reactieve metalen in groep 1 van de periodiek systeem (lithium, natrium, kalium, rubidium, cesium en francium).
* Ze hebben een sterke neiging om hun enkele valentie -elektron te verliezen, waardoor ze uitstekende reducerende middelen zijn.
* Wanneer alkali -metalen reageren met water, verplaatsen ze waterstof uit watermoleculen en vormen ze waterstofgas en een metaalhydroxide.
Hier is een algemene vergelijking voor de reactie:
2m + 2h₂o → 2mOH + H₂
Waar:
* M vertegenwoordigt een alkalimetaal.
* MOH vertegenwoordigt de metalen hydroxide.
Voorbeeld:
* Natrium (NA) reageren met water:
2na + 2h₂o → 2naOH + H₂
Deze reactie is zeer exotherme, wat betekent dat het veel warmte vrijgeeft, waardoor het waterstofgas zelfs kan ontbranden.
Opmerking: Andere metalen zoals calcium, magnesium en zink reageren ook met water om waterstofgas te produceren, maar ze vereisen specifieke omstandigheden, zoals verwarming of stoom.
 Is grafeen de beste warmtegeleider? Onderzoekers doen onderzoek met vier-fononverstrooiing
Is grafeen de beste warmtegeleider? Onderzoekers doen onderzoek met vier-fononverstrooiing  Welk gas zijn de reactanten in chemische reactant van fotosynthese?
Welk gas zijn de reactanten in chemische reactant van fotosynthese?  Wat zijn de waarnemingen als je ammoniummetavanadaat verwarmt in een nikkelkroes?
Wat zijn de waarnemingen als je ammoniummetavanadaat verwarmt in een nikkelkroes?  Wat betekent rood op de pH -schaal?
Wat betekent rood op de pH -schaal?  Welke voedingsmiddelen bevatten organische zuren?
Welke voedingsmiddelen bevatten organische zuren?
 Geiten:onwaarschijnlijke bondgenoten in Californië vechten tegen bosbranden
Geiten:onwaarschijnlijke bondgenoten in Californië vechten tegen bosbranden Beschrijf de interactie tussen een plant en zijn omgeving?
Beschrijf de interactie tussen een plant en zijn omgeving?  Zaadverspreiding in Mauritius – dood als een dodo?
Zaadverspreiding in Mauritius – dood als een dodo?  Bosbranden in Zuid-Californië laten gespleten persoonlijkheden zien
Bosbranden in Zuid-Californië laten gespleten persoonlijkheden zien  Gemeenschappelijk mineraal kan de sleutel zijn tot het aanpakken van klimaatverandering
Gemeenschappelijk mineraal kan de sleutel zijn tot het aanpakken van klimaatverandering
Hoofdlijnen
- Wat gorillapoep ons vertelt over evolutie en menselijke gezondheid
- Welke cellen zijn betrokken bij actieve immuniteit?
- Planten herprogrammeren hun cellen om indringers te bestrijden. Hier is hoe
- Wat maakt een koe een koe? Volledige rundergenoom gesequenced
- Gedragsstudies tonen aan dat bavianen en duiven in staat zijn tot cognitie op een hoger niveau
- Wat is een taak van sekscel?
- Groep organismen die het minst op elkaar lijken?
- Wat is de locatie van blaasjes die neurotransmitter opslaan?
- Kaketoes die bakken openen, gaan de wapenwedloop met mensen aan
- Onderzoekers rapporteren nieuwe hybride katalysator om water te splitsen

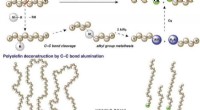
- Kunststoffen kunnen een tweede leven krijgen als biologisch afbreekbare oppervlakteactieve stoffen
- Bewaar ambachtelijk bier op een koele plaats en consumeer het zo vers mogelijk

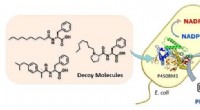
- Bacteriën misleiden om benzeen te hydroxyleren
- Krimpfolies krijgen grip

 Wat spoelwormen ons kunnen leren over menselijke groei?
Wat spoelwormen ons kunnen leren over menselijke groei? Waar is 34S breedtegraad 19e lengtegraad?
Waar is 34S breedtegraad 19e lengtegraad?  Lava overspoelt 100 huizen terwijl vulkaan Canarische Eilanden uitbarst
Lava overspoelt 100 huizen terwijl vulkaan Canarische Eilanden uitbarst Hoe zit het met de recente wilde tornado's? Deskundige weegt mee
Hoe zit het met de recente wilde tornado's? Deskundige weegt mee  Patches om het Sudo-hulpprogramma minder kwetsbaar te maken voor misbruik
Patches om het Sudo-hulpprogramma minder kwetsbaar te maken voor misbruik Hoe een ballonexperiment het werk van de Hubble-ruimtetelescoop kan doen
Hoe een ballonexperiment het werk van de Hubble-ruimtetelescoop kan doen  Gegevens over zwaartekrachtsgolven suggereren dat zwarte gaten van Goudlokje zeldzaam zijn
Gegevens over zwaartekrachtsgolven suggereren dat zwarte gaten van Goudlokje zeldzaam zijn Economische impact van kusterosie
Economische impact van kusterosie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

