
Wetenschap
Reageert cupric chloride met MG?
Hier is de evenwichtige chemische vergelijking:
cucl₂ (aq) + mg (s) → mgcl₂ (aq) + cu (s)
Verklaring:
* magnesium (mg) is reactiever dan koper (Cu) . Dit betekent dat het koper van zijn verbinding kan verplaatsen.
* In de reactie verliezen magnesiumatomen elk twee elektronen en worden magnesiumionen (mg²⁺) .
* Koperionen (Cu²⁺) van cupric chloride krijgen elk twee elektronen, die koperatomen (Cu) worden .
* De magnesiumionen combineren vervolgens met chloride -ionen (Cl⁻) om magnesiumchloride (mgcl₂) te vormen , die oplosbaar is in water.
Observaties:
* Je zou een roodbruine vaste (koper) die vormt op het oppervlak van het magnesiummetaal observeren.
* De oplossing zou waarschijnlijk van blauw veranderen (vanwege de aanwezigheid van Cu²⁺ -ionen) naar kleurloos (vanwege de aanwezigheid van mg²⁺ -ionen).
* De reactie kan warmte veroorzaken, wat een exotherme reactie aangeeft.
Opmerking: De reactie verloopt gemakkelijker als het magnesium zich in een poedervorm bevindt of als de oplossing wordt verwarmd.
 Een kleurrijke detector
Een kleurrijke detector Nieuwe flexibele en taaie superelastische metaallegering is veelbelovend in biomedische toepassingen
Nieuwe flexibele en taaie superelastische metaallegering is veelbelovend in biomedische toepassingen Onderzoeksteam introduceert een spectrum van potentiële vaccinadjuvantia
Onderzoeksteam introduceert een spectrum van potentiële vaccinadjuvantia  Het barsten van oliedruppels onder water:hoe vervuiling in het water kan achterblijven na het opruimen van lekkages
Het barsten van oliedruppels onder water:hoe vervuiling in het water kan achterblijven na het opruimen van lekkages  3 positieve ladingen en 4 negatieve, wat is de totale lading van een atoom?
3 positieve ladingen en 4 negatieve, wat is de totale lading van een atoom?
 Hoe reproduceren bomen zich?
Hoe reproduceren bomen zich?  P-22 leefde een episch en tragisch leven in Griffith Park:zou een nieuwe bergleeuw het beter doen?
P-22 leefde een episch en tragisch leven in Griffith Park:zou een nieuwe bergleeuw het beter doen?  Ruimtemijnbouw is geen sciencefiction, en Canada zou een prominente rol kunnen spelen
Ruimtemijnbouw is geen sciencefiction, en Canada zou een prominente rol kunnen spelen Niet zo met arendsogen:nieuw onderzoek onthult waarom vogels botsen met door de mens gemaakte objecten
Niet zo met arendsogen:nieuw onderzoek onthult waarom vogels botsen met door de mens gemaakte objecten  Wat doet een Killer Lake exploderen?
Wat doet een Killer Lake exploderen?
Hoofdlijnen
- Wat is het verschil tussen dizygote tweelingen en monozygote tweelingen?
- Wat zijn roofdieren van de gele spons?
- Hoe zenuwcellen verkeerd gevouwen eiwitten controleren
- Wetenschappers begrijpen hoe de E. coli-kloon wereldwijd verspreid is geraakt
- Welke neuronprocessen die normaal gesproken inkomende stimuli ontvangen, worden opgeroepen?
- Wat is wetenschap en zijn voorbeelden?
- Studie onderzoekt waarom sommige STEM-gebieden minder vrouwen hebben dan andere
- Hoe en waarom evolueerde homoseksueel gedrag bij mensen en andere dieren?
- Wat is een bio -indicator?
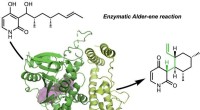
- Onderzoekers ontdekken eerste enzymen die een klassieke organische reactie katalyseren
- Over de aroma's van wijn piekeren

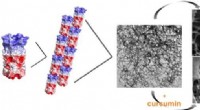
- Onderzoekers ontwikkelen thermo-responsieve eiwithydrogel
- Vlam aan! Hoe AI een complexe materiaaltechniek kan temmen en de productie kan transformeren

- Verven en lakken op basis van aardappelzetmeel

 Verstrengelde atomen schijnen eenstemmig
Verstrengelde atomen schijnen eenstemmig Hoe Chokecherries in het wild te identificeren
Hoe Chokecherries in het wild te identificeren Zelfassemblerende reagentia met instelbare kleuren en helderheid maken zeer multiplex tagging mogelijk, microscopische beeldvorming
Zelfassemblerende reagentia met instelbare kleuren en helderheid maken zeer multiplex tagging mogelijk, microscopische beeldvorming Het fijnste goudstof ter wereld
Het fijnste goudstof ter wereld Typen niet-gepolariseerde condensatoren
Typen niet-gepolariseerde condensatoren  Radiosignalen van verre sterren suggereren verborgen planeten
Radiosignalen van verre sterren suggereren verborgen planeten Hoe de waterkwaliteit in Europa te verbeteren
Hoe de waterkwaliteit in Europa te verbeteren  Als het gaat om de levering van medicijnen, Grootte doet er toe
Als het gaat om de levering van medicijnen, Grootte doet er toe
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

