
Wetenschap
Hoeveel aluminium atomen zijn er in een monstersulfide met massa 100 g?
1. Bepaal de chemische formule
Aluminiumsulfide bestaat uit aluminium (AL) en zwavel (s). De chemische formule voor aluminiumsulfide is Al₂s₃.
2. Bereken de molaire massa
* De molaire massa van aluminium (AL) is 26,98 g/mol.
* De molaire massa van zwavel (s) is 32,07 g/mol.
De molaire massa van al₂s₃ is:(2 * 26,98 g/mol) + (3 * 32.07 g/mol) =150,17 g/mol
3. Bereken het aantal mol
* We hebben een 100 g monster van Al₂s₃.
* Verdeel de monstermassa door de molaire massa om het aantal mol te krijgen:100 g / 150,17 g / mol =0,666 mol al₂s₃.
4. Bereken het aantal aluminiumatomen
* Elke mol van Al₂s₃ bevat 2 mol aluminiumatomen.
* Vermenigvuldig het aantal mol al₂s₃ met 2 om het aantal mol aluminium te krijgen:0,666 mol * 2 =1.332 mol aluminium.
* Gebruik het nummer van Avogadro (6.022 x 10²³ atomen/mol) om mol aluminium om te zetten in het aantal atomen:1.332 mol * 6.022 x 10²³ Atomen/mol = 8.02 x 10²³ Atomen van aluminium.
Daarom zijn er ongeveer 8,02 x 10²³ aluminiumatomen in een 100 g monster van aluminiumsulfide.
 Hoeveel kan suiker worden opgelost in een pot ml bij kamertemperatuur?
Hoeveel kan suiker worden opgelost in een pot ml bij kamertemperatuur?  Ammoniaksynthese - de grootste innovatie van de 20e eeuw
Ammoniaksynthese - de grootste innovatie van de 20e eeuw Op maat gemaakte verharding van bulkmetaalglas veroorzaakt door 2-D gradiëntverjonging
Op maat gemaakte verharding van bulkmetaalglas veroorzaakt door 2-D gradiëntverjonging Welke informatie is nodig om de pH in een oplossing te berekenen?
Welke informatie is nodig om de pH in een oplossing te berekenen?  Groot tinmonosulfidekristal opent weg voor volgende generatie zonnecellen
Groot tinmonosulfidekristal opent weg voor volgende generatie zonnecellen
 Vergeet slimme steden (voor een minuut), we moeten praten over slimme boerderijen
Vergeet slimme steden (voor een minuut), we moeten praten over slimme boerderijen Bugs kunnen een belangrijke indicator zijn voor de gezondheid van teruggewonnen bodem
Bugs kunnen een belangrijke indicator zijn voor de gezondheid van teruggewonnen bodem Wat is de naam om groene planten wit te worden door gebrek aan licht?
Wat is de naam om groene planten wit te worden door gebrek aan licht?  Vaardigheid en handicap:hoe we ze kunnen herkennen, hoe we het allemaal beter kunnen doen
Vaardigheid en handicap:hoe we ze kunnen herkennen, hoe we het allemaal beter kunnen doen  NASA's Terra Satellite vangt het einde van de tropische depressie Kulap
NASA's Terra Satellite vangt het einde van de tropische depressie Kulap
Hoofdlijnen
- Hoe de mitochondriën van een cel hun eigen eiwitfabrieken maken
- Een omkeerbare hoofdschakelaar ontdekken voor ontwikkeling
- Wat zijn de voorbeelden van antropoden?
- Gespecialiseerde cellen in het lichaam
- Wat zijn de functies van glazen schuif- en afdekglaasjes?
- Neanderthalers waren eigenlijk prehistorische Picasso's
- Wetenschappers ontdekken hoe planten grote wortelziekten bestrijden
- Wat maakt het endocriene systeem?
- Waarom noemde de wetenschapper Silver Argentum?
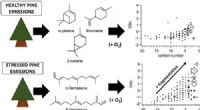
- Bladluis-gestresste dennen vertonen verschillende secundaire organische aerosolvorming
- Klikreactie voor levende systemen:Bioorthogonale hydroaminering van geactiveerde lineaire alkynen

- De zich snel ontvouwende toekomst van slimme stoffen

- Onderzoekers halen natuurlijk voorkomende melanine op grote schaal uit paddenstoelen

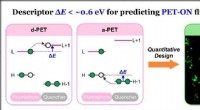
- Algemene descriptor zorgt voor vooruitgang in kleurstofchemie
 Hoe mollen naar moleculen te converteren
Hoe mollen naar moleculen te converteren Uit onderzoek blijkt dat merken weerbaar zijn tegen nepnieuws op sociale media
Uit onderzoek blijkt dat merken weerbaar zijn tegen nepnieuws op sociale media Neutronen schilderen atomair portret van prototypisch celsignaleringsenzym
Neutronen schilderen atomair portret van prototypisch celsignaleringsenzym Het manipuleren van rimpels kan leiden tot grafeenhalfgeleiders
Het manipuleren van rimpels kan leiden tot grafeenhalfgeleiders Hoe politiebewakingstechnologieën fungeren als instrumenten van blanke suprematie
Hoe politiebewakingstechnologieën fungeren als instrumenten van blanke suprematie Japan kondigt plannen aan om verbeterde observatiesatellieten te lanceren op de derde vlucht van nieuwe vlaggenschipraketten
Japan kondigt plannen aan om verbeterde observatiesatellieten te lanceren op de derde vlucht van nieuwe vlaggenschipraketten  Ingenieurs ontwikkelen 'slimme brillen' die automatisch scherpstellen op wat de drager ziet
Ingenieurs ontwikkelen 'slimme brillen' die automatisch scherpstellen op wat de drager ziet  Gebruik van plasmonics voor precisielandbouw wereldwijd
Gebruik van plasmonics voor precisielandbouw wereldwijd
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

