
Wetenschap
Mol van waterstof versus mol uranium?
Wat is een mol?
Een mol is een meeteenheid in de chemie. Het vertegenwoordigt een specifiek aantal deeltjes (atomen, moleculen, ionen, enz.). Dit nummer wordt het nummer van Avogadro genoemd, dat ongeveer 6.022 x 10^23 is.
Sleutelpunt: Een mol van elke stof bevat hetzelfde aantal deeltjes.
waterstof versus uranium
* waterstof (h): Eén mol waterstof bevat 6,022 x 10^23 waterstofatomen.
* uranium (u): Eén mol uranium bevat 6,022 x 10^23 uraniumatomen.
Het verschil
Hoewel beide hetzelfde aantal *deeltjes *bevatten, ligt het belangrijkste verschil in de *massa *van elke mol:
* waterstof is een zeer licht element. Eén mol waterstof heeft een massa van ongeveer 1 gram.
* Uranium is een zeer zwaar element. Eén mol uranium heeft een massa van ongeveer 238 gram.
Samenvattend:
* Hetzelfde aantal deeltjes: Eén mol waterstof en één mol uranium bevatten beide het aantal deeltjes van Avogadro.
* verschillende massa's: De massa van een mol waterstof is aanzienlijk minder dan de massa van een mol uranium vanwege het verschil in hun atoomgewichten.
Laat het me weten als je nog andere chemische vragen hebt!
 Natuurkundige maakt ademhalingstoestellen van het type N95 met een suikerspinmachine
Natuurkundige maakt ademhalingstoestellen van het type N95 met een suikerspinmachine Het pH-niveau van Ammoniak
Het pH-niveau van Ammoniak Is bisulfaat hetzelfde als hydrosulfaat?
Is bisulfaat hetzelfde als hydrosulfaat?  Wat is de chemische reactie tussen hcl en koh?
Wat is de chemische reactie tussen hcl en koh?  Onderzoekers ontwikkelen sterkere microben om de bioproductie van brandstoffen te verbeteren, Chemicaliën
Onderzoekers ontwikkelen sterkere microben om de bioproductie van brandstoffen te verbeteren, Chemicaliën
 Zijn papaverzaden slecht voor vogels?
Zijn papaverzaden slecht voor vogels?  Wat zijn enkele wetenschapskwaliteiten?
Wat zijn enkele wetenschapskwaliteiten?  Voorstel voor olieboringen voor Everglades kan moeilijker worden door de regering van Biden
Voorstel voor olieboringen voor Everglades kan moeilijker worden door de regering van Biden Nieuw inverse algoritme voor het ophalen van CO2 uit satellietwaarnemingen
Nieuw inverse algoritme voor het ophalen van CO2 uit satellietwaarnemingen De toekomst is nu:langetermijnonderzoek toont aan dat de verzuring van de oceaan op het Great Barrier Reef toeneemt
De toekomst is nu:langetermijnonderzoek toont aan dat de verzuring van de oceaan op het Great Barrier Reef toeneemt
Hoofdlijnen
- Gered Irrawaddy dolfijnkalf sterft ondanks wekenlange zorg
- Continentale controles nodig om de strijd tegen boomziekten te handhaven
- Twee factoren die het lot van een chemische reactie in levende cel bepalen?
- wat Eencellige organismen bestaan uit slechts één cel. Meercellig meer dan Welke levensfuncties kunnen zowel eencellige als meercellige organismen vervullen?
- Hersenloos,
- Draagt stikstofbases de genetische code voor specifiek?
- Waar wordt Myelin gevonden en wat zijn functie?
- Van polystyreenmicroplastics is aangetoond dat ze de invasie van exotische ondergedompelde macrofyten bevorderen
- Waarom worden benige vissen als omnivoren beschouwd in de visserijsport?
- Natures sweets:een natuurlijk recept lenen voor suikersynthese

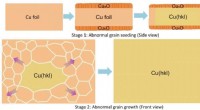
- Het afstemmen van het oppervlak geeft variaties op metaalfolies
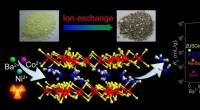
- Selectieve afvang van ionen uit afvalwater met gelaagd metaalsulfide
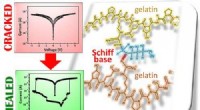
- Zelfherstellende folie op gelatinebasis kan een slimme zet zijn voor elektronica
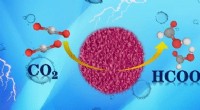
- Een voordelige aerogel op basis van legeringen als elektrokatalysator voor koolstoffixatie
 Het veel voorkomende gebruik van wijnsteenzuur
Het veel voorkomende gebruik van wijnsteenzuur IJs gedolven op Mars kan water opleveren voor mensen die de ruimte verkennen
IJs gedolven op Mars kan water opleveren voor mensen die de ruimte verkennen Tibet-sedimenten onthullen klimaatpatronen van miljoenen jaren geleden
Tibet-sedimenten onthullen klimaatpatronen van miljoenen jaren geleden Aardverschuiving Myanmar doodt 34, veel meer gevreesd vermist
Aardverschuiving Myanmar doodt 34, veel meer gevreesd vermist Welke soorten metingen worden gebruikt voor het meten in de ruimte?
Welke soorten metingen worden gebruikt voor het meten in de ruimte?  Waarom zou een pinniped in staat zijn om verder in water te reizen dan op het land?
Waarom zou een pinniped in staat zijn om verder in water te reizen dan op het land?  Voelt u zich sociaal angstig om terug te keren naar kantoor? Je bent niet de enige
Voelt u zich sociaal angstig om terug te keren naar kantoor? Je bent niet de enige  Als je lucht in het limoenwater blaast met een rietje, wat wordt waargenomen?
Als je lucht in het limoenwater blaast met een rietje, wat wordt waargenomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

