
Wetenschap
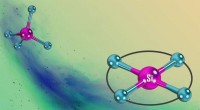
Waarom is een polair molecuul?
1. Elektronegativiteit:
* Verschillende atomen hebben verschillende vaardigheden om elektronen aan te trekken. Dit staat bekend als elektronegativiteit .
* Atomen met hogere elektronegativiteit trekken elektronen sterker aan.
* Wanneer twee atomen met verschillende elektronegativiteiten binden, worden de elektronen dichter bij het meer elektronegatieve atoom getrokken.
2. Polaire covalente bindingen:
* Wanneer een binding ontstaat tussen twee atomen met verschillende elektronegativiteiten, is de binding polaire covalent .
* This means the electrons are not shared equally, creating a partial positive charge Op het minder elektronegatieve atoom en een gedeeltelijke negatieve lading op het meer elektronegatieve atoom.
3. Moleculaire geometrie:
* Zelfs als een molecuul polaire covalente bindingen heeft, kan het niet Wees een polair molecuul. Dit hangt af van de geometrie van het molecuul.
* Om een molecuul polair te laten zijn, de gedeeltelijke ladingen moet worden gerangschikt op een manier die een ongelijke verdeling van lading over het gehele molecuul creëert.
* Bijvoorbeeld water (H 2 O) heeft twee polaire covalente bindingen (O-H). De gebogen geometrie van het molecuul zorgt ervoor dat de gedeeltelijke negatieve lading op het zuurstofatoom niet wordt geannuleerd door de gedeeltelijke positieve ladingen op de waterstofatomen. Dit creëert een netto dipoolmoment, waardoor water een polair molecuul is.
* Daarentegen koolstofdioxide (CO 2 ) heeft twee polaire covalente bindingen (C-O). De lineaire geometrie zorgt er echter voor dat de twee dipolen elkaar opzeggen, wat resulteert in een niet -polair molecuul.
Samenvattend:
* Een molecuul is polair als het polaire covalente bindingen heeft en een moleculaire geometrie Dat leidt tot een netto dipoolmoment .
* Dit resulteert in een scheiding van lading , het ene uiteinde van het molecuul enigszins positief maken en het andere uiteinde enigszins negatief.
Polaire moleculen zijn belangrijk omdat hun ongelijke ladingsverdeling hen in staat stelt om te interageren met andere polaire moleculen door dipool-dipool interacties . Deze interacties zijn cruciaal in veel biologische en chemische processen.
 Onderzoekers ontdekken dat zaadvliezen kunnen leiden tot sterke, moeilijk, maar toch flexibele materialen
Onderzoekers ontdekken dat zaadvliezen kunnen leiden tot sterke, moeilijk, maar toch flexibele materialen Wat zijn de vier belangrijkste organische verbindingen in levende wezens?
Wat zijn de vier belangrijkste organische verbindingen in levende wezens?  Wat is de juiste samengestelde naam voor Cu3n?
Wat is de juiste samengestelde naam voor Cu3n?  Hoe klein is een atoom?
Hoe klein is een atoom?  Wat is een schilderij op vers vochtige gips met pigmenten opgelost in water genoemd?
Wat is een schilderij op vers vochtige gips met pigmenten opgelost in water genoemd?
 Er vinden al 10 jaar bergtsunami's plaats, 000 jaar in Chileens Patagonië
Er vinden al 10 jaar bergtsunami's plaats, 000 jaar in Chileens Patagonië Giftige, voor altijd chemicaliën gevonden in kraanwater roepen vragen op voor wetenschappers
Giftige, voor altijd chemicaliën gevonden in kraanwater roepen vragen op voor wetenschappers Hoe het koopseizoen voor de feestdagen brandstof toevoegt aan een snel opwarmende planeet
Hoe het koopseizoen voor de feestdagen brandstof toevoegt aan een snel opwarmende planeet Wat is een gemeenschappelijke plant die wild wordt in Virginia?
Wat is een gemeenschappelijke plant die wild wordt in Virginia?  De groei van kolencentrales in Myanmar kan 280 doden, 000:studie
De groei van kolencentrales in Myanmar kan 280 doden, 000:studie
Hoofdlijnen
- Het orgaan in het lichaam absorbeert meer water is groot Instestine?
- Wat is een Thermobar?
- Wat zijn de twee belangrijkste soorten organismen?
- Onderzoekers onthullen hoe acetylering de centromeerdynamiek, chromosoomsegregatie en mitotische progressie reguleert
- Hittegolf veroorzaakt valse herfst in het VK
- Evolutie door natuurlijke selectie:voorbeelden en effecten van aanpassing
- De menselijke mannelijke gameet wordt een spermacel genoemd en geproduceerd in de?
- Uit welke soorten cellen bestaat bindweefsel?
- Is een groot stuk grasplant dier algen -schimmel?
- Zeesponzen inspireren de volgende generatie wolkenkrabbers en bruggen

- Nieuwe manier om ecstasy te detecteren ontdekt

- Silicium met een tweedimensionale structuur
- Massaspectrometriebeeldvorming maakt ingrediënten, additieven en contaminanten van voedsel zichtbaar

- Wetenschappers verbeteren het proces om moeilijk te recyclen plastic afval om te zetten in brandstof

 UITLEG:Waarom herbekijken scholen het hoogbegaafde onderwijs?
UITLEG:Waarom herbekijken scholen het hoogbegaafde onderwijs?  Runderembryo regenereert placenta-vormende cellen volledig
Runderembryo regenereert placenta-vormende cellen volledig Kan één aardbeving een cascade van meer veroorzaken?
Kan één aardbeving een cascade van meer veroorzaken? Nieuwe ontdekking om de ontwikkeling van zouttolerante wijnstokken te versnellen
Nieuwe ontdekking om de ontwikkeling van zouttolerante wijnstokken te versnellen Hoe PSI in KPa
Hoe PSI in KPa Hoe de doorlaatbaarheid te berekenen
Hoe de doorlaatbaarheid te berekenen Een magnetische oplossing om tumoren te identificeren en te doden
Een magnetische oplossing om tumoren te identificeren en te doden Wat bevat ertsen?
Wat bevat ertsen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

