
Wetenschap
Als water verzadigd is geraakt, blijft het zout oplost?
* Verzadigingspunt: Wanneer een oplossing zijn verzadigingspunt bereikt, betekent dit dat het de maximale hoeveelheid opgeloste stof (in dit geval zout) heeft opgelost dat deze bij een gegeven temperatuur en druk kan.
* evenwicht: Bij verzadiging bestaat er een dynamisch evenwicht. Dit betekent dat de snelheid van zout die in het water oplost gelijk is aan de snelheid van zout die uit de oplossing kristalliseert.
* Niet meer oplossen: Omdat de tarieven gelijk zijn, is er geen netto toename van de hoeveelheid opgelost zout. Elk extra toegevoegde zout wordt eenvoudig aan de onderkant van de container, niet opgelost.
Zie het als een spons:
* Een spons kan slechts een bepaalde hoeveelheid water absorberen voordat deze vol is.
* Evenzo kan water slechts een bepaalde hoeveelheid opgelost zout bevatten voordat het "vol" is.
Om meer zout op te lossen, zou je moeten:
* Verhoog de temperatuur: Hogere temperaturen zorgen over het algemeen mogelijk dat meer opgeloste stof oplost.
* Verander het oplosmiddel: Verschillende oplosmiddelen hebben verschillende oplosbaarheid voor zout.
* Verwijder wat water: Dit zou de concentratie van zout vergroten, waardoor de oplossing minder verzadigd is.
 Ontwikkelingsdilemma terwijl Oost-Groenland het toerisme stimuleert
Ontwikkelingsdilemma terwijl Oost-Groenland het toerisme stimuleert De veranderende rol van steden bij het aanpakken van de wereldwijde klimaatverandering
De veranderende rol van steden bij het aanpakken van de wereldwijde klimaatverandering Onderzoek onderzoekt de impact van koraalverbleking op de kustlijn van West-Australië
Onderzoek onderzoekt de impact van koraalverbleking op de kustlijn van West-Australië Bijgewerkte klimaatmodellen worden vertroebeld door wetenschappelijke vooroordelen, vinden onderzoekers
Bijgewerkte klimaatmodellen worden vertroebeld door wetenschappelijke vooroordelen, vinden onderzoekers Zijn planten geweldige voedselbron voor mens en andere dieren?
Zijn planten geweldige voedselbron voor mens en andere dieren?
Hoofdlijnen
- Wie is er bekend om ontdekkingen in radioactiviteit?
- Hoe snelheid de evolutionaire verandering van de wervelkolom bij zoogdieren beperkt
- Wat noemde Gregor Mendel de eigenschappen die verdwijnen in de eerste generatie?
- Slim boksen:de eenvoudige conserveringsstrategie om bedreigde Roseate sterns te redden
- Hoe wordt een enzym gedenatureerd?
- In vijverschuim, wetenschappers vinden antwoorden op een evolutie die het eerst kwam gevallen
- Voorbereid op oorlog:hoe cellen virale invasie overleven
- Hoe zijn sterk gevouwen membranen een voordeel voor de functies van cellulaire delen?
- Hoe produceert een plantencel een nieuwe wand tijdens cytokinese?
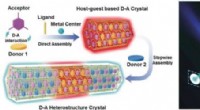
- Heterostructuurkristallen kunnen de weg naar optische circuits verlichten
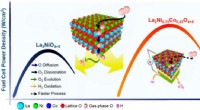
- Nieuw ontdekte ontwerpregels leiden tot betere brandstofcelkatalysator
- Nieuwe robotsensortechnologie kan reproductieve gezondheidsproblemen in realtime diagnosticeren

- Team vervaardigt magneten volledig van zeldzame aardmetalen uit de VS

- Nieuw, duurzame katalysator voor belangrijke brandstofcelreacties kan nuttig zijn in milieuvriendelijke voertuigen

 Wildvuurrook kan verbijsterende hoeveelheden schimmels en bacteriën bevatten, wetenschappers zeggen:
Wildvuurrook kan verbijsterende hoeveelheden schimmels en bacteriën bevatten, wetenschappers zeggen: Waarom Williamsons Synthese SN2 -mechanisme tonen?
Waarom Williamsons Synthese SN2 -mechanisme tonen?  Sferische weergave brengt virtuele samenwerking dichter bij de realiteit
Sferische weergave brengt virtuele samenwerking dichter bij de realiteit Hoe zou het proces worden genoemd dat energie vrijgeeft?
Hoe zou het proces worden genoemd dat energie vrijgeeft?  Beving Papoea-Nieuw-Guinea veroorzaakt kleine tsunami, geen schade
Beving Papoea-Nieuw-Guinea veroorzaakt kleine tsunami, geen schade Lijst in toenemende volgorde van smelttemperatuur HDPE PMMA LDPE?
Lijst in toenemende volgorde van smelttemperatuur HDPE PMMA LDPE?  Hubble toont een opmerkelijke galactische hybride
Hubble toont een opmerkelijke galactische hybride Effect van klimaatverandering op infectieziekten onbekend bij de helft van de bevolking
Effect van klimaatverandering op infectieziekten onbekend bij de helft van de bevolking
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

