
Wetenschap
Welke andere dingen lossen op in water?
Oplosbare verbindingen:
* zouten: De meeste zouten, zoals tafelzout (NaCl), lossen gemakkelijk op in water.
* suikers: Eenvoudige suikers zoals glucose en fructose lossen gemakkelijk op.
* zuren: Veel zuren, zoals zoutzuur (HCL) en zwavelzuur (H₂so₄), zijn zeer oplosbaar in water.
* Bases: Veel bases, zoals natriumhydroxide (NaOH) en kaliumhydroxide (KOH), zijn ook zeer oplosbaar.
* ethanol: Alcohol, zoals ethanol, is mengbaar met water, wat betekent dat ze in elke verhouding kunnen mengen.
Factoren die de oplosbaarheid beïnvloeden:
* polariteit: Water is een polair molecuul (het ene uiteinde is enigszins positief, het andere enigszins negatief). Stoffen met vergelijkbare polariteit aan water, zoals zouten en suikers, lossen goed op. Niet -polaire stoffen, zoals oliën, niet.
* Temperatuur: Over het algemeen verhoogt de toenemende temperatuur de oplosbaarheid voor de meeste vaste stoffen.
* Druk: Druk heeft een aanzienlijke invloed op de oplosbaarheid van gassen in vloeistoffen. Hogere druk verhoogt de oplosbaarheid.
Voorbeelden van gemeenschappelijke stoffen die oploven in water:
* zout (NaCl)
* suiker (c₁₂h₂₂o₁₁)
* azijn (azijnzuur)
* bakpoeder (natriumbicarbonaat)
* soap
* wasmiddel
* koffie
* thee
* sap
* veel medicijnen
Dingen die niet oplossen in water:
* oliën en vetten (niet -polair)
* zand
* Plastic
* hout
Onthoud: Oplost is een complex proces dat door vele factoren wordt beïnvloed. Sommige stoffen lossen slechts gedeeltelijk op en vormen oplossingen met een limiet aan hoeveel opgeloste stof bij een gegeven temperatuur kan worden opgelost.
 Onderzoekers berekenen hoe riviernetwerken zich door een landschap bewegen
Onderzoekers berekenen hoe riviernetwerken zich door een landschap bewegen  NASA vindt een zwakkere Sarai nu een depressie
NASA vindt een zwakkere Sarai nu een depressie Het traceren van de geschiedenis van de landbouw in heel Afrika geeft aanwijzingen voor lage productie-outputs
Het traceren van de geschiedenis van de landbouw in heel Afrika geeft aanwijzingen voor lage productie-outputs Snelle verkenning na de aardbeving van Anchorage in 2018 onthult tekenen van grondfalen
Snelle verkenning na de aardbeving van Anchorage in 2018 onthult tekenen van grondfalen Ozonchemie meten in een bewoonde woning
Ozonchemie meten in een bewoonde woning
Hoofdlijnen
- Je bent wat je eet – als je een koraalrifvis bent
- Veerkracht van boomsoorten getest onder klimaatopwarming
- Waar vind je DNA- en erfelijkheidsinformatie voor de cel?
- Studie biedt een eerste verklaring voor hoe cellen snel hun structuur herstellen en behouden
- Wat zijn de vier belangrijkste delen van het metabolisme?
- In welk orgelsysteem is rectus abdominus?
- Virussen bestrijden:codebrekers worden codeschrijvers
- Waar komen haarcellen daar nuritioment vandaan?
- Onderzoekers leren waarom in het water levende zoogdieren groot moeten zijn, maar niet té groot
- Chemicus creëert efficiënte katalysator voor synthese van organische sulfiden

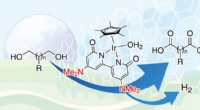
- Team synthetiseert gelijktijdig dicarbonzuren en waterstof uit diolen
- Visualisatie van moleculaire beweging van gesubstitueerd 9-fosfaanthraceen

- Omringd door potentieel:nieuwe wetenschap bij het omzetten van biomassa
- Brandstofaërosolen die de vervuiling van het milieu verminderen

 Welke Amerikaanse staat ligt het dichtst bij waar de eerste mensen een landbrug naar Noord -Amerika hebben overgestoken?
Welke Amerikaanse staat ligt het dichtst bij waar de eerste mensen een landbrug naar Noord -Amerika hebben overgestoken?  Cryovulkanisme:waarom bestuderen? Wat kan het ons leren over het vinden van leven buiten de aarde?
Cryovulkanisme:waarom bestuderen? Wat kan het ons leren over het vinden van leven buiten de aarde?  Hemelse kat ontmoet kosmische kreeft
Hemelse kat ontmoet kosmische kreeft Zeep van stro - wetenschappers ontwikkelen milieuvriendelijk ingrediënt uit landbouwafval
Zeep van stro - wetenschappers ontwikkelen milieuvriendelijk ingrediënt uit landbouwafval Volcano Eruption Experiments
Volcano Eruption Experiments  In welke minerale groep zit ijs?
In welke minerale groep zit ijs?  Welke stap komt alvorens een experiment uit te voeren in de wetenschappelijke methode.
Welke stap komt alvorens een experiment uit te voeren in de wetenschappelijke methode.  Een mobiele overstromingstool voor de natie onthuld
Een mobiele overstromingstool voor de natie onthuld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

