
Wetenschap
Welke elementenfamilie verliest het gemakkelijkst elektronen?
Dit is waarom:
* Elektronische configuratie: Alkali -metalen hebben slechts één valentie -elektron in hun buitenste schaal.
* Lage ionisatie -energie: Ze hebben een relatief lage ionisatie -energie, wat betekent dat er minder energie voor nodig is om dat elektron met enkele valentie te verwijderen.
* elektropositiviteit: Alkali -metalen zijn zeer elektropositief, wat betekent dat ze een sterke neiging hebben om elektronen te verliezen en positieve ionen (kationen) te vormen.
Voorbeeld: Natrium (NA) verliest gemakkelijk zijn ene valentie -elektron om een Na+ ion te vormen.
Laat het me weten als je meer details wilt over een van deze concepten!
 Welke elementen maken aluminiumsulfaat?
Welke elementen maken aluminiumsulfaat?  Waarom verandert een vaste stof in vloeistof wanneer warmte wordt toegevoegd?
Waarom verandert een vaste stof in vloeistof wanneer warmte wordt toegevoegd?  Hoe tatoeages werken
Hoe tatoeages werken  Wat veroorzaakt die piek? Beantwoording van een al lang bestaande vraag over covalente vloeistoffen
Wat veroorzaakt die piek? Beantwoording van een al lang bestaande vraag over covalente vloeistoffen  Chemici ontwikkelen nieuw materiaal waarmee slim glas in recordtijd van kleur kan veranderen
Chemici ontwikkelen nieuw materiaal waarmee slim glas in recordtijd van kleur kan veranderen
 Dominante planten in een tropisch regenwoud
Dominante planten in een tropisch regenwoud Microplastics kunnen overvloedig aanwezig zijn in de oppervlaktesedimenten van Baynes Sound en Lambert Channel
Microplastics kunnen overvloedig aanwezig zijn in de oppervlaktesedimenten van Baynes Sound en Lambert Channel De Indonesische Mount Ruang barst opnieuw uit, waarbij as wordt uitgestoten en dorpen worden bezaaid met puin
De Indonesische Mount Ruang barst opnieuw uit, waarbij as wordt uitgestoten en dorpen worden bezaaid met puin  Hoe Californië de terugdraaiing van het milieu van Trump blijft blokkeren
Hoe Californië de terugdraaiing van het milieu van Trump blijft blokkeren Waarom sommige groene beleidsmaatregelen de vooruitgang op het gebied van klimaatverandering daadwerkelijk kunnen vertragen
Waarom sommige groene beleidsmaatregelen de vooruitgang op het gebied van klimaatverandering daadwerkelijk kunnen vertragen
Hoofdlijnen
- Waarom is een academisch woord?
- Bestaat er zoiets als een werkelijk onzelfzuchtige daad?
- Biobrandstoffen als invasieve soort?
- AI-aangedreven virtuele rat biedt inzicht in hoe hersenen complexe, gecoördineerde bewegingen controleren
- Wat is een eigenschap heeft twee allelen die worden weergegeven door p en q als 0,89 wat q is?
- Baby bongo geboren, waarschijnlijk binnenkort in Species Survival Center
- Wat is een bijtmiddel in de microbiologie?
- UW-wetenschappers ontrafelen het mysterie van hoe griepvirussen zich vermenigvuldigen
- Wat is mRNA? u moet op de hoogte zijn van het belangrijkste ingrediënt in sommige COVID-19-vaccins
- Nieuwe benadering van terpeensynthese
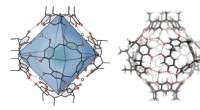
- Nieuwe materialen voor duurzame, goedkope batterijen

- Wetenschappers ontwerpen supersnelle moleculaire motor
- Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede

- Onderzoekers maken de eerste rietjes met polyhydroxyalkanoaat (PHA) plastic

 Hoe Bracket-schimmels aan hun eigen voedsel komen?
Hoe Bracket-schimmels aan hun eigen voedsel komen?  Welke twee categorieën worden gebruikt om deeltjes te classificeren?
Welke twee categorieën worden gebruikt om deeltjes te classificeren?  De top 10-onderwerpen voor onderzoeksdocumenten
De top 10-onderwerpen voor onderzoeksdocumenten  Facebook schorst Canadees bedrijf te midden van dataminingschandaal
Facebook schorst Canadees bedrijf te midden van dataminingschandaal Intel:Hot Chips-evenementdetails AI-krachtige processors
Intel:Hot Chips-evenementdetails AI-krachtige processors Verdringen bruine weduwen zwarte weduwenspinnen rond huizen in Zuid-Californië?
Verdringen bruine weduwen zwarte weduwenspinnen rond huizen in Zuid-Californië?  Nieuwe nanolijm is dun en superkleverig
Nieuwe nanolijm is dun en superkleverig Waarom reizen soundwaves sneller door vaste stoffen?
Waarom reizen soundwaves sneller door vaste stoffen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

