
Wetenschap
Is NH4NO3 N2O H2O een disproportioneringsreactie?
Dispruptionation -reactie: Een disproportioneringsreactie is een redox -reactie waarbij hetzelfde element zowel oxidatie als reductie ondergaat.
Analyse van de reactie:
* nh₄no₃ → n₂o + 2h₂o
1. Stikstof in NH₄NO₃: Stikstof heeft een oxidatietoestand van -3 in ammonium (NH₄⁺) en +5 in nitraat (NO₃⁻).
2. stikstof in n₂o: Stikstof heeft een oxidatietoestand van +1 in stikstofoxide (N₂O).
3. stikstof in h₂o: Stikstof is niet aanwezig in water.
Observatie: In deze reactie is stikstof in de reactant (NH₄NO₃) aanwezig in twee verschillende oxidatietoestanden (-3 en +5). In het product heeft stikstof (N₂O) een oxidatietoestand van +1. Dit betekent:
* stikstof in ammonium (NH₄⁺) wordt geoxideerd: Van -3 tot +1.
* stikstof in nitraat (NO₃⁻) is verminderd: Van +5 tot +1.
Conclusie: Omdat hetzelfde element (stikstof) zowel oxidatie als vermindering van de reactie ondergaat, wordt het geclassificeerd als een disproportioneringsreactie.
 Waarom is molecuulmassa belangrijk?
Waarom is molecuulmassa belangrijk?  Onderzoeksteam introduceert een spectrum van potentiële vaccinadjuvantia
Onderzoeksteam introduceert een spectrum van potentiële vaccinadjuvantia  Wat zijn alternatieve materialen voor ureum formaldehyde?
Wat zijn alternatieve materialen voor ureum formaldehyde?  Wat is niobium, een vaste vloeistof of gas?
Wat is niobium, een vaste vloeistof of gas?  Wat is het verschil tussen het verdunnen van een geconcentreerde oplossing met behulp van de termen opgeloste stof en oplosmiddel?
Wat is het verschil tussen het verdunnen van een geconcentreerde oplossing met behulp van de termen opgeloste stof en oplosmiddel?
Hoofdlijnen
- Wat zijn de twee verschillende stadia van meiose?
- Wat voor soort circulatiesysteem heeft een schimmels?
- Waarom mensen niet zo egocentrisch zijn, zou je denken – nieuw onderzoek
- Het ontrafelen van de metabolische mysteries van grasmatten onder hittestress
- Wat komt er na een organen?
- Waarom is water een essentieel onderdeel van het leven?
- Hoe bieden nucleotiden nucleisch met specifieke codes?
- Welke ziekten zijn het gevolg van een abnormale celfunctie?
- Waarom zijn het allemaal levende wezens afkomstig van een gewone of universele voorouder?
- De vonk die het leven schiep
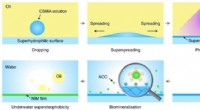
- Onderzoekers maken op parelmoer geïnspireerde superoleofobe onderwaterfilms
- Banden die binden, en kan worden losgemaakt
- Vanille maakt melkdranken zoeter

- Onderzoekers om te onderzoeken of metaalcorroderende microben kunnen groeien in de voorgestelde nucleaire afvalfaciliteit van Canada

 Flexibiliteit en rangschikking - de interactie van ribonucleïnezuur en water
Flexibiliteit en rangschikking - de interactie van ribonucleïnezuur en water Nieuwe microscoop vestigt een record voor het visualiseren van oppervlaktebevochtigende eigenschappen
Nieuwe microscoop vestigt een record voor het visualiseren van oppervlaktebevochtigende eigenschappen Gegevens van teledetectie werpen licht op wanneer en hoe asteroïde Ryugu zijn water verloor
Gegevens van teledetectie werpen licht op wanneer en hoe asteroïde Ryugu zijn water verloor  Botten uit de ijstijd teruggevonden in onderwatergrotten in Mexico
Botten uit de ijstijd teruggevonden in onderwatergrotten in Mexico Het is onwaarschijnlijk dat de jacht op trofeeën de evolutie beïnvloedt
Het is onwaarschijnlijk dat de jacht op trofeeën de evolutie beïnvloedt Video:zeeniveau in kaart brengen vanuit de ruimte
Video:zeeniveau in kaart brengen vanuit de ruimte Onderzoek wijst op verdubbeling van het rijbereik voor elektrische voertuigen
Onderzoek wijst op verdubbeling van het rijbereik voor elektrische voertuigen Dodental van Filippijnse storm, aardverschuivingen klimmen naar 126
Dodental van Filippijnse storm, aardverschuivingen klimmen naar 126
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

