
Wetenschap
Is de snelheid van de reactie beïnvloed door het hoeveelheid enzym in de omgeving?
* Enzymen zijn katalysatoren: Ze versnellen de reacties zonder in het proces te worden geconsumeerd.
* Actieve sites: Enzymen hebben specifieke actieve plaatsen waar reactanten (substraten) binden en een chemische transformatie ondergaan.
* Beperkte actieve sites: Het aantal actieve locaties die beschikbaar zijn op enzymmoleculen is eindig.
* Verzadiging: Naarmate de substraatconcentratie toeneemt, neemt de reactiesnelheid toe totdat alle actieve plaatsen bezet zijn. Op dit punt is het enzym verzadigd en het toevoegen van meer substraat zal de reactiesnelheid niet verder verhogen.
De relatie:
* Lage enzymconcentratie: Met een lage enzymconcentratie zijn er minder actieve locaties beschikbaar, dus de reactiesnelheid zal langzamer zijn.
* Hoge enzymconcentratie: Met een hogere enzymconcentratie zijn er meer actieve locaties beschikbaar, dus de reactiesnelheid zal sneller zijn (totdat het enzym verzadigd is).
Key Takeaways:
* Verhoogde enzymconcentratie =verhoogde reactiesnelheid (tot verzadiging)
* verlaagde enzymconcentratie =verlaagde reactiesnelheid
Denk er zo aan: Stel je een druk restaurant voor met slechts een paar koks. Als u meer koks (enzymen) toevoegt, kan het restaurant sneller meer mensen (reactanten) serveren. Zelfs met meer koks is er echter een limiet aan hoe snel ze kunnen werken. Zodra de koks allemaal bezet zijn, zal het toevoegen van meer klanten het restaurant niet sneller laten lopen.
 Wat is de reactie tussen natriumhydroxide en calciumbicarbonaat?
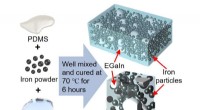
Wat is de reactie tussen natriumhydroxide en calciumbicarbonaat?  Nieuwe methode stimuleert de vorming van syngas uit biopolyolen
Nieuwe methode stimuleert de vorming van syngas uit biopolyolen Heeft isomeren dezelfde fysische en chemische eigenschappen?
Heeft isomeren dezelfde fysische en chemische eigenschappen?  Moleculaire hopper klein genoeg om enkele DNA-strengen te verplaatsen
Moleculaire hopper klein genoeg om enkele DNA-strengen te verplaatsen Wat is het chemische proces dat de productie van ontvlambare dampen uit vaste houtbrandstoffen veroorzaakt?
Wat is het chemische proces dat de productie van ontvlambare dampen uit vaste houtbrandstoffen veroorzaakt?
Hoofdlijnen
- Hoe worden organismen geclassificeerd op basis van het aantal cellen?
- Afrikaanse gewassen bieden een voedzame, glutenvrije oplossing
- Milieubeheer van inheemse naties bij het aanpakken van invasieve soorten
- Wat is een palindroom in relatie tot de restrictie-enzymplaats?
- Hoe verschilt STP van ATP?
- Wat is Hermisphere?
- Hoe lepra werkt
- Hoe rifvissen de cyclus van de maan kunnen gebruiken om het geslacht van hun nakomelingen te manipuleren
- Wat is een mogelijk voordeel van genetisch gemodificeerde gewassen?
- Kunnen we grafiet maken van steenkool? Onderzoekers beginnen met het vinden van nieuwe vaste koolstof

- Team ontdekt dubbele helixstructuur in synthetisch macromolecuul

- Detectie van meerdere sepsis-biomarkers uit volbloed - snel gemaakt, nauwkeurig, en goedkoop

- Nieuw slim materiaal werkt beter onder druk
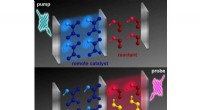
- Chemische reacties aansturen via afstandsbediening
 Rapport:Federale Facebook-sonde omvat nu FBI, SEC
Rapport:Federale Facebook-sonde omvat nu FBI, SEC Wat vertelt atomaire massa ons?
Wat vertelt atomaire massa ons?  Syngenta schikt Amerikaanse boerenrechtszaken in Chinese maïshandelzaak
Syngenta schikt Amerikaanse boerenrechtszaken in Chinese maïshandelzaak Lewis John Stadler
Lewis John Stadler  Lipoproteïnen gedragen zich bijna als een kleine klittenbandbal
Lipoproteïnen gedragen zich bijna als een kleine klittenbandbal Voorbereiding op een menselijke missie naar Mars
Voorbereiding op een menselijke missie naar Mars Onderzoekers om te ontwerpen, instrument bouwen om metalen asteroïde te verkennen
Onderzoekers om te ontwerpen, instrument bouwen om metalen asteroïde te verkennen Hoe is het noordoosten deel van ons geworden?
Hoe is het noordoosten deel van ons geworden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

