
Wetenschap
Hoeveel mol H2O worden geproduceerd wanneer 0,468 mol octaan wordt verbrand?
Hier is hoe dit probleem op te lossen:
1. Schrijf de gebalanceerde chemische vergelijking voor de verbranding van octaan:
C₈h₁₈ + 25/2 o₂ → 8 co₂ + 9 h₂o
2. Bepaal de molverhouding tussen octaan en water:
Uit de evenwichtige vergelijking zien we dat 1 mol octaan (c₈h₁₈) 9 mol water produceert (H₂o).
3. Bereken de geproduceerde mol water:
* Gebruik de molverhouding om mol octaan om te zetten in watermole:
0,468 mol C₈h₁₈ * (9 mol H₂o / 1 mol C₈h₁₈) = 4.212 mol H₂o
Daarom worden 4.212 mol water geproduceerd wanneer 0,468 mol octaan wordt verbrand.
 Welke drankjes laten het ijs het snelst smelten en waarom?
Welke drankjes laten het ijs het snelst smelten en waarom?  Wetenschappers vinden nieuw solid-state materiaal voor thermische regeling
Wetenschappers vinden nieuw solid-state materiaal voor thermische regeling Nieuwe technologie om bittere amandelen in realtime te detecteren
Nieuwe technologie om bittere amandelen in realtime te detecteren Levert CO2-etikettering ontwikkelingslanden een slechte deal op?
Levert CO2-etikettering ontwikkelingslanden een slechte deal op?  Wie voorspelde eerst het bestaan van een atoom?
Wie voorspelde eerst het bestaan van een atoom?
 NASA's Suomi NPP-satelliet toont twee weergaven van de rokerige luchten van Californië
NASA's Suomi NPP-satelliet toont twee weergaven van de rokerige luchten van Californië Een habitat Shoebox maken Diorama
Een habitat Shoebox maken Diorama Cycloon Mekenu treft Jemenitische eiland, zeven vermist
Cycloon Mekenu treft Jemenitische eiland, zeven vermist Hoe ESA Zuid-Afrika helpt water eerlijk te delen
Hoe ESA Zuid-Afrika helpt water eerlijk te delen Pesticiden die in contact komen met plastic mulch hebben meer tijd nodig om af te breken
Pesticiden die in contact komen met plastic mulch hebben meer tijd nodig om af te breken
Hoofdlijnen
- Waarom denk je dat Linnaeus geen classificatiekoninkrijken heeft opgenomen voor categorieën archaea en bacteriën?
- Hoe overleeft een plant met weinig partners of bestuivers? Een Europees kruid heeft zijn eigen weg gevonden
- Wat is accumulatie van verontreinigende stoffen op opeenvolgende niveaus de voedselketen.?
- Er zijn nieuwe details onthuld over hoe planten een optimale sperma-ei-verhouding behouden
- Hoe een celmodel te maken met Playdough
- wat Eencellige organismen bestaan uit slechts één cel. Meercellig meer dan Welke levensfuncties kunnen zowel eencellige als meercellige organismen vervullen?
- Is de term cerebrale dominantie het halfrond aan dat dominant is voor taal?
- Morfologisch en biochemisch bewijs vergelijken ter ondersteuning van evolutie?
- Zebravissen laten zien hoe bio-elektriciteit de spierontwikkeling beïnvloedt
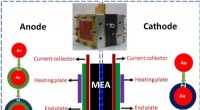
- Onderzoekers ontwikkelen selectieve elektrokatalysatoren om de prestaties van directe methanol-brandstofcellen te verbeteren
- Robotachtige zachte materie buigt, draait en kruipt wanneer geraakt met licht

- Ademtests kunnen COVID-19 opsporen
- Massaspectrometrietechniek helpt bij het identificeren van vervalste manuscripten van Robert Burns

- Zo mooi als een pauw:de edelsteen voor de volgende generatie slimme sensoren

 Dichtstbijzijnde exoplaneet tot nu toe bevestigd door European Southern Observatory
Dichtstbijzijnde exoplaneet tot nu toe bevestigd door European Southern Observatory  Beoordeling van het wereldwijde probleem van slechte sanitaire voorzieningen
Beoordeling van het wereldwijde probleem van slechte sanitaire voorzieningen Hoe LB's per SEC te converteren naar CFM
Hoe LB's per SEC te converteren naar CFM Politie zwart gat ontdekt een slapend zwart gat buiten het Melkwegstelsel
Politie zwart gat ontdekt een slapend zwart gat buiten het Melkwegstelsel Wat is de dichtheid van gneis?
Wat is de dichtheid van gneis?  Door docenten te laten kiezen wat ze willen leren, wordt het moreel van de docenten ondersteund – en wordt er beter onderwijs gegeven
Door docenten te laten kiezen wat ze willen leren, wordt het moreel van de docenten ondersteund – en wordt er beter onderwijs gegeven  NASA-gegevens tonen aan dat Florence stortregens en recordoverstromingen naar de Carolinas brengt
NASA-gegevens tonen aan dat Florence stortregens en recordoverstromingen naar de Carolinas brengt Celbeweging Welke structuur doet dit?
Celbeweging Welke structuur doet dit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

