
Wetenschap
Wat is het verschil tussen een isotoop en ion van hetzelfde element?
isotopen
* Definitie: Atomen van hetzelfde element met hetzelfde aantal protonen (atoomnummer) maar een ander aantal neutronen.
* Key -kenmerken:
* Hetzelfde atoomnummer: Dit definieert het element.
* ander massanummer: Het massagummer is de som van protonen en neutronen.
* chemische eigenschappen: Isotopen van hetzelfde element hebben over het algemeen zeer vergelijkbare chemische eigenschappen, omdat hun elektronenconfiguraties hetzelfde zijn.
* Voorbeeld: Carbon-12 (6 protonen, 6 neutronen) en koolstof-14 (6 protonen, 8 neutronen) zijn koolstof isotopen.
ionen
* Definitie: Atomen of moleculen die elektronen hebben gewonnen of verloren, wat resulteert in een netto elektrische lading.
* Key -kenmerken:
* Hetzelfde atoomnummer: Het aantal protonen blijft hetzelfde en definieert het element.
* Verschillende aantal elektronen: Dit creëert de positieve of negatieve lading.
* chemische eigenschappen: Ionen hebben aanzienlijk verschillende chemische eigenschappen in vergelijking met hun neutrale atoomtegenhangers vanwege de verandering in elektronenconfiguratie en lading.
* Voorbeeld: Een natriumatoom (NA) heeft 11 protonen en 11 elektronen. Wanneer het één elektron verliest, wordt het een natriumion (Na+), dat 11 protonen en 10 elektronen heeft.
In een notendop:
* isotopen verschillen in het aantal neutronen, wat leidt tot verschillende atoommassa's.
* ionen verschillen in het aantal elektronen, wat leidt tot een positieve of negatieve lading.
Laat het me weten als u meer specifieke isotoop- of ionenvoorbeelden in meer detail wilt verkennen!
 Langetermijnmetingen laten zien hoe het klimaat verandert
Langetermijnmetingen laten zien hoe het klimaat verandert  De natuur helpt de geestelijke gezondheid, zegt onderzoek – maar alleen voor rijke, blanke mensen?
De natuur helpt de geestelijke gezondheid, zegt onderzoek – maar alleen voor rijke, blanke mensen?  De bossen in Ghana worden weggevaagd:wat zit hierachter en waarom pogingen om dit te stoppen niet werken?
De bossen in Ghana worden weggevaagd:wat zit hierachter en waarom pogingen om dit te stoppen niet werken?  Gegevens over zweten van planten kunnen helpen bij het voorspellen van de ernst van natuurbranden
Gegevens over zweten van planten kunnen helpen bij het voorspellen van de ernst van natuurbranden Dammen of niet dammen? Pakistan-experts denken na over de overstromingsstrategie
Dammen of niet dammen? Pakistan-experts denken na over de overstromingsstrategie
Hoofdlijnen
- Hoe is een Cells DNA net als de boeken in een bibliotheek?
- Waar kwam DNA -informatie vandaan als er geen God is?
- Wat zijn de verschillen tussen een plant en een dierlijke cel onder een microscoop?
- Waarom bevatten de testen veel glad ER?
- Hoe cellen hun mRNA-voorraad en de output ervan beheren
- Discovery onthult hoe planten cellulose maken voor kracht en groei
- Wat zijn de monomeren van triglyceriden?
- Hoe transcriptiefactoren het genoom verkennen
- Hoe grootte cellen splitst:Cellen meten het oppervlak om te weten wanneer ze delen
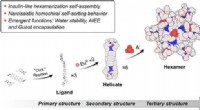
- Hexamere lanthanide-organische capsules met tertiaire structuur, opkomende functies
- Mysterieuze micro-eiwitten hebben grote gevolgen voor menselijke ziekten
- Wat maakt de dodelijke kogelvis zo verrukkelijk?

- De ontwikkeling van bacteriën markeert een nieuw tijdperk in cellulair ontwerp
- Laser volgt therapieën, voedingsstoffen, gifstoffen

 Laat in video's de ivoorsnavelspecht zien, of is deze uitgestorven?
Laat in video's de ivoorsnavelspecht zien, of is deze uitgestorven? De coronale sluier:zijn de magnetische bogen van de zon een optische illusie?
De coronale sluier:zijn de magnetische bogen van de zon een optische illusie? Welke andere elementen dan koolstof zijn gebruikt om een mol te definiëren?
Welke andere elementen dan koolstof zijn gebruikt om een mol te definiëren?  Hoeveel ml zijn gelijk aan 75 mg?
Hoeveel ml zijn gelijk aan 75 mg?  Zelfassemblage van complexe systemen:zeshoekige bouwstenen zijn beter
Zelfassemblage van complexe systemen:zeshoekige bouwstenen zijn beter  Waarom is het zo moeilijk voor mensen om een baby te krijgen?
Waarom is het zo moeilijk voor mensen om een baby te krijgen? Het ontwerpen van complexe structuren die de mogelijkheden van conventionele lithografie te boven gaan
Het ontwerpen van complexe structuren die de mogelijkheden van conventionele lithografie te boven gaan Apertiefbeelden leveren eerste wetenschappelijke resultaten op
Apertiefbeelden leveren eerste wetenschappelijke resultaten op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

