
Wetenschap
Waarom lossen verwarmde oplosmiddelen sneller opgeloste opgeloste stof op?
1. Verhoogde kinetische energie: Het verwarmen van een oplosmiddel verhoogt de kinetische energie van zijn moleculen. Dit betekent dat ze sneller bewegen en vaker en botsen met de opgeloste deeltjes en met een grotere kracht. Deze botsingen breken de opgeloste deeltjes uit, waardoor hun oppervlak vergroten en ze gemakkelijker beschikbaar maken voor solvatie.
2. Verzwakking van intermoleculaire krachten: Het verwarmen van een oplosmiddel verzwakt de intermoleculaire krachten (zoals waterstofbruggen, dipool-dipoolinteracties, enz.) Tussen oplosmiddelmoleculen. Hierdoor kunnen de oplosmiddelmoleculen gemakkelijker omringen en interageren met de opgeloste deeltjes.
3. Verhoogde diffusie: Naarmate de kinetische energie van de oplosmiddelmoleculen toeneemt, diffunderen ze sneller. Hierdoor kunnen ze de opgeloste deeltjes sneller bereiken en sneller beginnen met het solvatieproces.
4. Verhoogde oplosbaarheid: In veel gevallen neemt de oplosbaarheid van een opgeloste stof in een oplosmiddel toe met de temperatuur. Dit betekent dat een hogere concentratie van de opgeloste stof kan oplossen in het verwarmde oplosmiddel in vergelijking met het koude oplosmiddel.
Samenvattend:
Het verwarmen van een oplosmiddel biedt in wezen meer energie voor het solvatieproces, waardoor de oplosmiddelmoleculen effectiever kunnen communiceren met de opgeloste deeltjes en sneller oplossen.
Opmerking: Het specifieke effect van temperatuur op oplosbaarheid hangt af van de aard van de opgeloste stof en oplosmiddel. Sommige stoffen vertonen een toename van de oplosbaarheid met temperatuur, terwijl anderen een daling kunnen vertonen of relatief constant kunnen blijven.
 3D-geprinte Biomesh minimaliseert hernia-reparatiecomplicaties
3D-geprinte Biomesh minimaliseert hernia-reparatiecomplicaties Is Pledge een zuur of een base?
Is Pledge een zuur of een base?  Verrode fluorescerende zijde kan schadelijke bacteriën doden als biomedische en milieuremedie
Verrode fluorescerende zijde kan schadelijke bacteriën doden als biomedische en milieuremedie Nieuwe tool kan bloedinfecties snel behandelen
Nieuwe tool kan bloedinfecties snel behandelen Slimme diëlektrische elastomeren voor zelfherstellende zachte robots
Slimme diëlektrische elastomeren voor zelfherstellende zachte robots
 Potentieel schadelijke ozonniveaus aan het oppervlak stegen tijdens lockdown
Potentieel schadelijke ozonniveaus aan het oppervlak stegen tijdens lockdown Hoeveel mensen zullen migreren als gevolg van de stijgende zeespiegel? Onze beste gissingen zijn niet goed genoeg
Hoeveel mensen zullen migreren als gevolg van de stijgende zeespiegel? Onze beste gissingen zijn niet goed genoeg Australië moet de wereld leiden op het gebied van natuurherstel door middel van een ambitieuze interpretatie van het internationaal recht
Australië moet de wereld leiden op het gebied van natuurherstel door middel van een ambitieuze interpretatie van het internationaal recht  Arctische lekkage zorgt voor opschudding bij Russische mijnbouwgigant
Arctische lekkage zorgt voor opschudding bij Russische mijnbouwgigant Nieuwe manier om jaarringen te analyseren bevestigt ongekende opwarming in Centraal-Azië
Nieuwe manier om jaarringen te analyseren bevestigt ongekende opwarming in Centraal-Azië
Hoofdlijnen
- Hoe een ontevreden wetenschapper wilde bewijzen dat zijn voedsel niet nieuw ontdekte radioactieve tracers was en de Nobelprijs won
- Een andere massale verblekingsgebeurtenis verwoest het Great Barrier Reef. Wat is er nodig om koraal te laten overleven?
- Zijdehaai maakt recordbrekende migratie in de internationale wateren van de tropische oostelijke Stille Oceaan
- Chlamydiae vergroot onze kijk op hoe intracellulaire bacteriën evolueren
- Nieuwe krachtdetectiemethode onthult hoe cellen weefselstijfheid waarnemen
- Bewijs dat energiemetabolisme en regulatie van biofilmvorming in bacteriën met elkaar verweven zijn
- Wat veroorzaakt een chromosoominversie?
- Ontdekken hoe een vleesetende schimmel wormen vangt en verteert
- Wat is de trotosfeer?
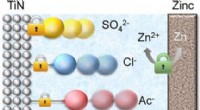
- Zink-ion hybride condensatoren met ideale anionen in de elektrolyt vertonen extra lange prestaties
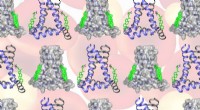
- Cholesterol helpt het griepvirus te ontsnappen door het membraan van de gastheercel
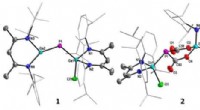
- Toekomstige opties voor het opslaan van koolstofdioxide:Synthese van anorganische heteroalkenen
- Een chemische aanwijzing voor hoe het leven op aarde begon

- Samenstellingsontwerp van legeringen met meerdere componenten door screening met hoge doorvoer

 Sterke markten voor kweekvlees in vleesverminderend Duitsland en Frankrijk
Sterke markten voor kweekvlees in vleesverminderend Duitsland en Frankrijk Het timen van de levensduur van antimateriedeeltjes kan leiden tot een betere behandeling van kanker
Het timen van de levensduur van antimateriedeeltjes kan leiden tot een betere behandeling van kanker Wat zei de wiskundeleraar na acht uur in ijs- en sneeuwstorm te hebben doorgebracht?
Wat zei de wiskundeleraar na acht uur in ijs- en sneeuwstorm te hebben doorgebracht?  Afstudeerder bedenkt eenvoudige, goedkope techniek om het materiaal van de toekomst te onderzoeken
Afstudeerder bedenkt eenvoudige, goedkope techniek om het materiaal van de toekomst te onderzoeken Bij welke temperatuur lost ammoniak op in water?
Bij welke temperatuur lost ammoniak op in water?  Hoe kunt u een elektrische ventilator repareren die niet goed werkt, een wetenschappelijke methode toepassen?
Hoe kunt u een elektrische ventilator repareren die niet goed werkt, een wetenschappelijke methode toepassen?  Zijn methylkationen stabieler dan ethylkationen?
Zijn methylkationen stabieler dan ethylkationen?  Studie vindt directe verbanden tussen oude koolstof, grafiet en hydrothermale ventilatieopeningen op de zeebodem
Studie vindt directe verbanden tussen oude koolstof, grafiet en hydrothermale ventilatieopeningen op de zeebodem
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

