
Wetenschap
Wat is de wortelgemiddelde snelheid van heliumatoom in één mol Een ideaal gas bij een druk 2,00 atmosferen en temperatuur 30 graden C. a Hij heeft massa 4U?
1. Converteren eenheden
* Temperatuur: 30 ° C =303,15 K (voeg 273.15 toe om van Celsius naar Kelvin te converteren)
* Druk: 2,00 atm =2,03 x 10^5 PA (1 atm =1.01325 x 10^5 PA)
* massa: 4 u =6,64 x 10^-27 kg (1 u =1.66054 x 10^-27 kg)
2. Gebruik de ideale gaswet
De ideale gaswet relateert druk (P), volume (V), aantal mol (N), de ideale gasconstante (R) en temperatuur (T):
PV =NRT
We kunnen dit gebruiken om het volume te vinden:
V =(nrt)/p
3. Bereken de RMS -snelheid
De wortelgemaakte snelheid (V_RMS) van een ideaal gas wordt gegeven door:
v_rms =√ (3rt/m)
Waar:
* R is de ideale gasconstante (8.314 J/(mol · k)))
* T is de temperatuur in Kelvin
* M is de molaire massa van het gas in kg/mol (m =4 g/mol =0,004 kg/mol voor helium)
Berekeningen
1. Zoek het volume:
V =(1 mol * 8.314 j / (mol · k) * 303.15 k) / (2.03 x 10^5 pa)
V ≈ 0,0124 m³
2. Bereken de RMS -snelheid:
v_rms =√ (3 * 8.314 j/(mol · k) * 303.15 k/0.004 kg/mol)
v_rms ≈ 1360 m/s
Daarom is de wortelgemiddelde snelheid van heliumatomen in één mol van een ideaal gas bij een druk van 2,00 atmosferen en een temperatuur van 30 graden Celsius is ongeveer 1360 m/s
 Wat hebben kalium en Krypton gemeen?
Wat hebben kalium en Krypton gemeen?  Zullen ijzer en chloor een ionische verbinding vormen?
Zullen ijzer en chloor een ionische verbinding vormen?  Greenwashen of juist doen? Corporate dilemma’s op COP28
Greenwashen of juist doen? Corporate dilemma’s op COP28  Scheuren maken historische schilderijen minder kwetsbaar voor omgevingsvariaties
Scheuren maken historische schilderijen minder kwetsbaar voor omgevingsvariaties Onderzoekers bepalen de structuur van nieuw metaaltelluraatmateriaal met mogelijke toepassingen in zonne-energie en meer
Onderzoekers bepalen de structuur van nieuw metaaltelluraatmateriaal met mogelijke toepassingen in zonne-energie en meer
 Bronnen van nieuwe ozonbeschadigende HCFK's terug te voeren tot hun oorsprong
Bronnen van nieuwe ozonbeschadigende HCFK's terug te voeren tot hun oorsprong Bewoners verdeeld over toekomst van Roemeense vuilnisbelt-tijdbom
Bewoners verdeeld over toekomst van Roemeense vuilnisbelt-tijdbom De twee belangrijkste factoren die het klimaat bepalen, zijn?
De twee belangrijkste factoren die het klimaat bepalen, zijn?  Welke invloed hebben lokale droge meren op de luchtkwaliteit en de menselijke gezondheid?
Welke invloed hebben lokale droge meren op de luchtkwaliteit en de menselijke gezondheid?  De oorsprong van fijnstofvervuiling in Guangzhou, China
De oorsprong van fijnstofvervuiling in Guangzhou, China
Hoofdlijnen
- Een botanisch mysterie opgelost door fylogenetische tests
- Is er zoiets als eiwitpil?
- Wat is een alomtegenwoordig in de voedselketen?
- Nieuw genomisch onderzoek biedt een glimp van hoe walvissen zich kunnen aanpassen aan de oceaan
- Welke dieren zijn dagelijkse?
- Is de term cerebrale dominantie het halfrond aan dat dominant is voor taal?
- Longorganoïden onthullen hoe ziekteverwekkers menselijk longweefsel infecteren
- Wanneer moet u uw hond castreren of steriliseren? Onderzoekers actualiseren richtlijnen
- Wat is de rol van enzymen in het metabolisme?
- Duurzame chemie op kwantumniveau

- De suikercode kraken - waarom de glycoom het volgende grote ding is in gezondheid en geneeskunde
- Onderzoek onthult microbiële bedreiging voor belangrijke voedingsstof
- Bevindingen bevestigen het vermogen van beeldvormende technieken om gezond weefsel te onderscheiden na neoadjuvante chemotherapie
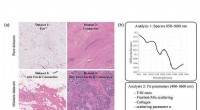
- Prestaties van vaste katalysator voor methaanomzetting worden voorspeld door theoretische berekening
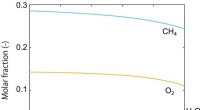
 Russische raket lanceert Britse telecomsatellieten
Russische raket lanceert Britse telecomsatellieten EU-klimaatwetgeving een stap in de goede richting onderzoekers zeggen:
EU-klimaatwetgeving een stap in de goede richting onderzoekers zeggen: Hoe meet je 3 gallons?
Hoe meet je 3 gallons?  Topologische grafeen nanoribbons vangen elektronen op voor nieuwe kwantummaterialen
Topologische grafeen nanoribbons vangen elektronen op voor nieuwe kwantummaterialen Intel lanceert derde patch voor strijd tegen MDS Goliath
Intel lanceert derde patch voor strijd tegen MDS Goliath Natuurkundigen ontdekken eenvoudig voortstuwingsmechanisme voor lichamen in dichte vloeistoffen
Natuurkundigen ontdekken eenvoudig voortstuwingsmechanisme voor lichamen in dichte vloeistoffen De kans op eenzaamheid van mensen kan tot de helft afnemen als steden 30% groene ruimtedoelstellingen halen
De kans op eenzaamheid van mensen kan tot de helft afnemen als steden 30% groene ruimtedoelstellingen halen Wat is een stof met een massa van 6,48 g en een volume van 3 cm?
Wat is een stof met een massa van 6,48 g en een volume van 3 cm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

