
Wetenschap
Hoeveel mol gas zijn aanwezig wanneer het volume 100,0 liter druk 3 atmosferen en temperatuur -10c is?
1. Converteren eenheden
* temperatuur (t): Convert Celsius naar Kelvin:
T (k) =t (° C) + 273.15
T (k) =-10 ° C + 273.15 =263.15 k
2. Ideale gaswet
De ideale gaswet is:
PV =NRT
Waar:
* P =druk (in atmosferen)
* V =volume (in liters)
* n =aantal mol
* R =ideale gasconstante (0,0821 l · atm/mol · k)
* T =temperatuur (in kelvin)
3. Oplossen voor n (aantal mol)
Herschik de ideale gaswet om op te lossen voor n:
n =PV / RT
4. Sluit de waarden aan aan
n =(3 atm * 100,0 l) / (0,0821 l · atm / mol · k * 263.15 k)
5. Berekenen
n ≈ 13.9 mol
Daarom zijn ongeveer 13,9 mol gas aanwezig onder deze omstandigheden.
 Hoe noem je een koolzuurhoudend drankje dat de toonkracht en de functie van een orgel verbetert?
Hoe noem je een koolzuurhoudend drankje dat de toonkracht en de functie van een orgel verbetert?  Gigantische moleculen in de vorm van Kandinsky-cirkels zijn giftig voor MRSA-bacteriën
Gigantische moleculen in de vorm van Kandinsky-cirkels zijn giftig voor MRSA-bacteriën Franse wetenschappers beweren metallische waterstof te hebben gemaakt
Franse wetenschappers beweren metallische waterstof te hebben gemaakt Bacterieval kan antibioticaresistentie helpen vertragen
Bacterieval kan antibioticaresistentie helpen vertragen Quantumcomputers verbeteren
Quantumcomputers verbeteren
 De effecten van klimaatverandering op watertekorten
De effecten van klimaatverandering op watertekorten Levenscyclus van een cricket
Levenscyclus van een cricket Verschuivende oceaanstromingen stuwen steeds meer warmte naar de koelere wateren van het zuidelijk halfrond
Verschuivende oceaanstromingen stuwen steeds meer warmte naar de koelere wateren van het zuidelijk halfrond Hoe de Tibetaanse verheffing de evolutie van de westelijke circulatie beïnvloedt
Hoe de Tibetaanse verheffing de evolutie van de westelijke circulatie beïnvloedt De complete levenscyclus van de Giant Panda
De complete levenscyclus van de Giant Panda
Hoofdlijnen
- Wat is de rol van enzymcomplex in de elektrontransportketen?
- Wat zijn enkele materialen die ik zou kunnen gebruiken om plantencellen te maken?
- Retrovirus versus DNA-virus
- Vindt natuurlijke selectie plaats in tegenstelling tot evolutie?
- Wat zijn drie primaire doelen van mitose?
- Wat is de samenvatting voor ei in flessexperiment?
- Waarom begon Mendel zijn experimenten door eren te laten pollineren voor meerdere generaties?
- Waarom is biologie belangrijk in de studie van de psychologie?
- Wat zijn de verschillen tussen een plant en een dierlijke cel onder een microscoop?
- Vermindering van het corrosieve effect van gesmolten zouten

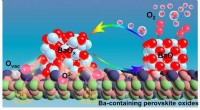
- Mechanisme van zuurstofactivering op bariumbevattende perovskietmaterialen
- Een manier om onderkoeling te overwinnen

- Het mysterie van gedegradeerde reel-to-reel-tapes ontrafelen

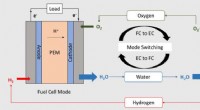
- Nieuwe katalysator helpt brandstofcel te combineren, batterij in één apparaat
 Waarom de menselijke stem zo veelzijdig is
Waarom de menselijke stem zo veelzijdig is  De wetenschap bevindt zich in een reproduceerbaarheidscrisis:hoe lossen we deze op?
De wetenschap bevindt zich in een reproduceerbaarheidscrisis:hoe lossen we deze op?  Welke eigenschap wordt uitgedrukt wanneer twee verschillende genen voor hetzelfde aanwezig zijn opgeroepen?
Welke eigenschap wordt uitgedrukt wanneer twee verschillende genen voor hetzelfde aanwezig zijn opgeroepen?  Wat is de nuttige uitgangsenergie van een tafelventilator?
Wat is de nuttige uitgangsenergie van een tafelventilator?  Gigantische paraplu's verschuiven van handige luifel naar stevig stormscherm
Gigantische paraplu's verschuiven van handige luifel naar stevig stormscherm Kan uw hond een aardbeving voorspellen? Het bewijs is wankel, zeggen onderzoekers
Kan uw hond een aardbeving voorspellen? Het bewijs is wankel, zeggen onderzoekers  Efficiënte generatie van relativistische mid-infraroodpulsen in de buurt van een cyclus in plasma's
Efficiënte generatie van relativistische mid-infraroodpulsen in de buurt van een cyclus in plasma's Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen
Onderzoek onthult waarom het moeilijk is om de geur uit polyester te krijgen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

