
Wetenschap
Wat wordt er in een chemische reactie geschreven als deze in balans is?
Dit is wat je niet wijziging:
* chemische formules: U verandert nooit de subscripts binnen de chemische formules zelf. Dit zou de identiteit van de verbinding veranderen.
Voorbeeld:
onevenwichtig: H₂ + O₂ → H₂o
uitgebalanceerd: 2h₂ + o₂ → 2h₂o
In dit voorbeeld hebben we een coëfficiënt van "2" toegevoegd voor H₂ en H₂o om het aantal waterstof- en zuurstofatomen aan beide zijden van de vergelijking in evenwicht te brengen.
Waarom balanceren we chemische reacties?
Het balanceren van chemische reacties is cruciaal omdat het ervoor zorgt dat:
* De wet van het behoud van massa wordt gehoorzaamd: De totale massa van de reactanten moet gelijk zijn aan de totale massa van de producten.
* De juiste molverhoudingen worden weergegeven: Hierdoor kunt u nauwkeurig de hoeveelheden reactanten en producten voorspellen die bij een reactie betrokken zijn.
* De reactie is stoichiometrisch nauwkeurig: Dit betekent dat de reactie verloopt met de juiste verhoudingen van reactanten en producten.
 De donkere kant van de lente? Vervuiling in onze smeltende sneeuw
De donkere kant van de lente? Vervuiling in onze smeltende sneeuw  Bioraffinaderijen zullen slechts minimale effecten hebben op de markten voor houtproducten en grondstoffen
Bioraffinaderijen zullen slechts minimale effecten hebben op de markten voor houtproducten en grondstoffen Nieuw onderzoek naar brandbeheersing richt zich op risico en veiligheid
Nieuw onderzoek naar brandbeheersing richt zich op risico en veiligheid Hoe snelwegbruggen zingen (of kreunen) in de regen om hun gezondheid te onthullen
Hoe snelwegbruggen zingen (of kreunen) in de regen om hun gezondheid te onthullen  Wat is de UV-index? Een expert legt uit wat het betekent en hoe het wordt berekend
Wat is de UV-index? Een expert legt uit wat het betekent en hoe het wordt berekend
Hoofdlijnen
- Welke klassen van biologische moleculen worden het gemakkelijkst geabsorbeerd en gemetaboliseerd door gist?
- Wat is synaptische varicositeit die verwijst naar hoe veranderingen in sensibilisatie van Aplysia?
- Stamboom van Homo Sapiens blijft evolueren
- Elektronenmicroscoopbeelden laten zien hoe cellen een essentieel mineraal absorberen
- Waarom is Thomas Edison een beroemde wetenschapper?
- Soorten instrumenten die worden gebruikt voor het meten van lichaamstemperaturen
- Afnemende bijenpopulaties:een natuurverschijnsel of een waarschuwing?
- Moet u uw huisdier rauw vlees voeren? De echte risico's van een 'traditioneel' hondendieet
- Noem de drie organen die zaadvloeistof produceren?
- De kern van hoe uien je aan het huilen maken
- Onderzoekers vinden potentiële nieuwe bron van zeldzame aardelementen

- Onderzoekers identificeren breekpunt van geleidend materiaal

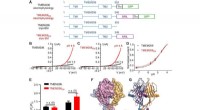
- Cryo-elektronenmicroscopische structuur van een proton-geactiveerd chloridekanaal genaamd TMEM206
- Selectieve oplossing van elementair goud uit multimetaalbronnen in organische oplossingen

 Wat vertegenwoordigt het lint op dekking van Eclipse?
Wat vertegenwoordigt het lint op dekking van Eclipse?  Onderzoekers observeren nieuwe isotoop van fluor
Onderzoekers observeren nieuwe isotoop van fluor Onderzoekers proberen nieuwe methode om verontreinigde sedimenten te reinigen
Onderzoekers proberen nieuwe methode om verontreinigde sedimenten te reinigen Smakelijk of verrot? Een afstotende geur remt de perceptie van een aangename azijnvlieg
Smakelijk of verrot? Een afstotende geur remt de perceptie van een aangename azijnvlieg  Wat geeft een meer accurate beeld van de aarde - kaart of wereldbol uitleggen?
Wat geeft een meer accurate beeld van de aarde - kaart of wereldbol uitleggen?  Spark joy:gebruik de op Marie Kondo geïnspireerde methode om uw smartphone op te ruimen, tablet en laptop
Spark joy:gebruik de op Marie Kondo geïnspireerde methode om uw smartphone op te ruimen, tablet en laptop Three Main Types of Galaxies
Three Main Types of Galaxies Wat zijn de oorzaken van de ontwikkeling van landvormen op aarde?
Wat zijn de oorzaken van de ontwikkeling van landvormen op aarde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

