Wetenschap
Wat is de deeltjestheorie van materie voor water koken?
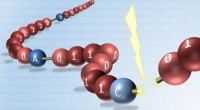
1. Watermoleculen in vloeibare toestand:
* Watermoleculen bewegen constant en trillen.
* Ze zijn dicht bij elkaar en hebben een sterke aantrekkingskracht op elkaar (waterstofbinding). Deze aantrekkingskracht houdt ze in vloeibare toestand.
2. Warmte toevoegen:
* Wanneer warmte wordt toegevoegd aan water, absorberen de moleculen energie.
* Deze energie zorgt ervoor dat de moleculen sneller trillen en verder uit elkaar bewegen.
3. Breaking Bonds:
* Naarmate de moleculen sneller bewegen, overwinnen ze de aantrekkelijke krachten tussen hen (waterstofbruggen).
* De bindingen tussen watermoleculen breken.
4. Overgang naar gas:
* Wanneer voldoende energie wordt geabsorbeerd, worden de moleculen ver genoeg uit elkaar dat ze uit de vloeibare toestand ontsnappen en waterdamp worden (gas).
* Deze gasmoleculen bewegen vrij en willekeurig, met zeer zwakke attracties naar elkaar.
5. Kookpunt:
* Het kookpunt van water (100 ° C of 212 ° F) is de temperatuur waarbij de dampdruk van het water gelijk is aan de atmosferische druk.
* Dit betekent dat de watermoleculen voldoende energie hebben om de druk van de omringende lucht te overwinnen en als gas in de atmosfeer te ontsnappen.
Sleutelpunten:
* Verhoogde kinetische energie: De belangrijkste factor bij het koken is de toename van de kinetische energie van de watermoleculen als gevolg van warmteabsorptie.
* dampdruk: De druk die wordt uitgeoefend door de waterdamp boven de vloeistof neemt toe naarmate de temperatuur stijgt.
* Faseverandering: Koken is een fysieke toestandsverandering van vloeistof naar gas.
Visualiseren het:
Stel je wat watermoleculen voor als kleine, trillende ballen. Wanneer je ze verwarmt, beginnen ze meer wild rond te stuiteren, uiteindelijk loskomen van hun buren en stoom worden.
 Onderzoekers introduceren programmeerbare materialen om gebroken botten te helpen genezen
Onderzoekers introduceren programmeerbare materialen om gebroken botten te helpen genezen  Bacteriën die giftige metalen binden:zijn zij de toekomst van het opruimen van kernafval?
Bacteriën die giftige metalen binden:zijn zij de toekomst van het opruimen van kernafval?  Georganiseerde chaos in het enzymcomplex - verrassende inzichten en nieuwe perspectieven
Georganiseerde chaos in het enzymcomplex - verrassende inzichten en nieuwe perspectieven Is Germanium een dirigent of een isolator?
Is Germanium een dirigent of een isolator?  Lokaal meten van de pH met terahertz-spectroscopie
Lokaal meten van de pH met terahertz-spectroscopie
 Hoe helpen aerosolen onze atmosfeer om zichzelf te reinigen?
Hoe helpen aerosolen onze atmosfeer om zichzelf te reinigen? Korpsfunctionaris:studie nodig van de overstromingsopties van de Missouri River
Korpsfunctionaris:studie nodig van de overstromingsopties van de Missouri River Antropogene luchtvervuiling heeft invloed op de gezondheid en het klimaat in het Midden-Oosten
Antropogene luchtvervuiling heeft invloed op de gezondheid en het klimaat in het Midden-Oosten Onderzoekers brengen hoge niveaus van drugs in de Hudson River in kaart
Onderzoekers brengen hoge niveaus van drugs in de Hudson River in kaart Wat dacht hij? Studie wendt zich tot apenintellect
Wat dacht hij? Studie wendt zich tot apenintellect
Hoofdlijnen
- Welk soort mutatie heeft het grotere potentieel om de evolutie een populatiebodycel of in een eiercel te beïnvloeden?
- Wat zijn enkele biotische factoren van gist?
- Hoe werkt de kernbeheersingsfuncties van het leven?
- Wanneer worden twee populaties beschouwd als nieuwe en afzonderlijke soorten?
- Wat maakt iets wetenschappelijk?
- Onderzoek onthult nieuw inzicht in hoe cheeta's hun prooi vangen
- Hoe overleeft het blauwtongvirus de winter?
- Helpt aminozuren ons om te groeien?
- Welk monomeer wordt gevonden in amandelen maar geen RNA?
 Kleine deeltjes die wolken kunnen vormen uit sporengassen boven open zee
Kleine deeltjes die wolken kunnen vormen uit sporengassen boven open zee Onderzoeken hoe geavanceerde materialen veilig en duurzaam moeten zijn
Onderzoeken hoe geavanceerde materialen veilig en duurzaam moeten zijn  Biologen ontdekken hoe planten stamcellen reconstrueren
Biologen ontdekken hoe planten stamcellen reconstrueren  Waarom hebben we schrikkeljaren?
Waarom hebben we schrikkeljaren?  Hoe naar dinosaurussporen te kijken
Hoe naar dinosaurussporen te kijken  Onderzoeksteam ontdekt nieuwe eigenschap van licht
Onderzoeksteam ontdekt nieuwe eigenschap van licht  Methode om de moleculaire distributie van MXene te meten maakt kwaliteitscontrole in het productieproces mogelijk
Methode om de moleculaire distributie van MXene te meten maakt kwaliteitscontrole in het productieproces mogelijk  Welke eiwitten in zoogdieren vertonen alleen primaire en secundaire structuren?
Welke eiwitten in zoogdieren vertonen alleen primaire en secundaire structuren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com