
Wetenschap
Wat zijn de elementen in groep 17 van het periodiek systeem?
* fluor (f)
* chloor (Cl)
* bromine (br)
* jodium (i)
* astatine (AT)
* tennessine (ts)
Key -kenmerken van halogenen:
* zeer reactieve niet -metalen: Ze vormen gemakkelijk verbindingen met andere elementen, vooral metalen.
* bestaan als diatomaire moleculen: Ze worden in de natuur gevonden als paren van atomen (bijv. CL₂, Br₂).
* Souten vormen met metalen: De halogenen reageren met metalen om ionische verbindingen te vormen die zouten worden genoemd.
* elektronegatief: Ze hebben een sterke neiging om elektronen aan te trekken.
* Variërende toestanden bij kamertemperatuur: Fluor en chloor zijn gassen, broom is een vloeistof en jodium is een vaste stof.
* belangrijk in biologische systemen: Halogenen spelen cruciale rollen in de menselijke gezondheid, zoals chloor in desinfectiemiddelen en jodium bij de productie van schildklierhormoon.
 Temperatuur, tijd en bosbessenwijn:onderzoekers onderzoeken de effecten van fermentatie op gezondheidsbevorderende stoffen
Temperatuur, tijd en bosbessenwijn:onderzoekers onderzoeken de effecten van fermentatie op gezondheidsbevorderende stoffen  Welke vloeistof zal een nagel roesten?
Welke vloeistof zal een nagel roesten?  Team ontwikkelt beeldvormingshulpmiddel voor kanker van paardenkastanjes
Team ontwikkelt beeldvormingshulpmiddel voor kanker van paardenkastanjes Nieuw model beschrijft fasescheiding die antilichaamoplossingen bederft
Nieuw model beschrijft fasescheiding die antilichaamoplossingen bederft Hoe gebruik je het wetenschappelijke woord atoom in een zin?
Hoe gebruik je het wetenschappelijke woord atoom in een zin?
 Juli 2019 warmste maand ooit voor planeet:NOAA
Juli 2019 warmste maand ooit voor planeet:NOAA Nieuwe studie onderzoekt de oorzaken en gevolgen van de overstromingen in Wimberley in 2015
Nieuwe studie onderzoekt de oorzaken en gevolgen van de overstromingen in Wimberley in 2015 Instandhouding van tropische veengebieden kan mensen beschermen tegen nieuwe ziekten
Instandhouding van tropische veengebieden kan mensen beschermen tegen nieuwe ziekten Het verminderen van vervuiling veroorzaakt geen piek in de opwarming van de aarde, studie vondsten
Het verminderen van vervuiling veroorzaakt geen piek in de opwarming van de aarde, studie vondsten Zijn de belangrijkste factoren die een temperatuur beïnvloeden, de heersende wind en bergen?
Zijn de belangrijkste factoren die een temperatuur beïnvloeden, de heersende wind en bergen?
Hoofdlijnen
- Genomisch onderzoek helpt bij het begrijpen hoe dodelijke schimmelinfecties kunnen worden behandeld
- Onderzoek naar diergedrag kan beter voorkomen dat vooringenomenheid van waarnemers binnensluipt, maar er is nog steeds ruimte voor verbetering
- Hoe een eiwit vrijkomt om dodelijke kankers te veroorzaken
- Onderzoekers krijgen inzicht in hoe ultrakleine bacteriën uit de omgeving zich hebben aangepast om in mensen te leven
- Welk lichaamssysteem beschermt de terugbereiken buitenlandse stoffen?
- Wetenschappers:woestijnschildpad bedreigd, 100 over in Arizona
- Wat is de naam van het maken van mRNA Copt A Gene?
- Wat zijn de vijf verschillende bewijslijnen voor evolutie?
- Welke stoffen helpen de lichaamsfuncties te reguleren?
- Onderzoekers synthetiseren nieuwe vloeibare kristallen die gerichte transmissie van elektriciteit mogelijk maken

- Onderzoekers ontwikkelen een nieuw type synthetische moleculaire machine
- Nieuwe flexibele en taaie superelastische metaallegering is veelbelovend in biomedische toepassingen

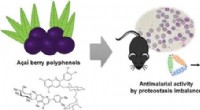
- Aaí bessenextracten bestrijden malaria bij muizen
- Nieuwe methode maakt de weg vrij voor snijgereedschappen met een langere levensduur

 Hoe was de grote grote rode plek op Jupiter gevormd?
Hoe was de grote grote rode plek op Jupiter gevormd?  Wanneer dupliceren chromosomen tijdens een cellevenscyclus?
Wanneer dupliceren chromosomen tijdens een cellevenscyclus?  Een metaaldetector voor onderzoek selecteren
Een metaaldetector voor onderzoek selecteren μkiss:een nieuwe methode voor het nauwkeurig afleveren van nanodeeltjes en kleine moleculen aan individuele cellen
μkiss:een nieuwe methode voor het nauwkeurig afleveren van nanodeeltjes en kleine moleculen aan individuele cellen  Chemici gebruiken gemodificeerde DNA-nucleotiden om nieuwe materialen te maken
Chemici gebruiken gemodificeerde DNA-nucleotiden om nieuwe materialen te maken Wanneer een cel zich splitst in twee genetisch identieke dochtercellen?
Wanneer een cel zich splitst in twee genetisch identieke dochtercellen?  Het fabricageproces zorgt voor lage kosten, duurzame optie voor voedselverpakkingen
Het fabricageproces zorgt voor lage kosten, duurzame optie voor voedselverpakkingen Onderzoekers stemmen wrijving in ionische vaste stoffen af op nanoschaal
Onderzoekers stemmen wrijving in ionische vaste stoffen af op nanoschaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

