
Wetenschap
Waarom is SiO2 meer oplosbaar in zeewater versus zoet water?
* zoutgehalte: Zeewater bevat een hoge concentratie opgeloste zouten, voornamelijk natriumchloride (NaCl). Deze zouten verhogen de ionsterkte van de oplossing, waardoor het voor SiO2 moeilijker is om op te lossen.
* ionische interacties: De opgeloste ionen in zeewater concurreren met SiO2 voor hydratatie (het proces van watermoleculen rond en stabiliserende ionen/moleculen). Deze concurrentie vermindert de effectieve waterconcentratie die beschikbaar is voor het oplossen van SiO2.
* complexering: Sommige van de opgeloste ionen in zeewater, zoals calcium (ca²⁺), kunnen complexen vormen met opgeloste silica, waardoor het effectief uit de oplossing wordt verwijderd.
Samenvattend: Het hoge zoutgehalte en de ionsterkte van zeewater maken het een minder gunstige omgeving voor het oplossen van SiO2 in vergelijking met zoet water.
Opmerking: Hoewel SiO2 minder oplosbaar is in zeewater dan in zoet water, worden beide nog steeds als relatief laag in oplosbaarheid beschouwd. De overgrote meerderheid van silica in de oceaan bestaat in de vorm van vaste deeltjes (bijv. Diatomeeën).
 Welk gas wordt gebruikt om bruis in koolzuurhoudende dranken te doen?
Welk gas wordt gebruikt om bruis in koolzuurhoudende dranken te doen?  Welke elementen heeft de minste waarde voor elektro-negativiteit lithium of Krypton?
Welke elementen heeft de minste waarde voor elektro-negativiteit lithium of Krypton?  Wetenschappers fabriceren veelzijdige katalysator voor polyestersynthese en -afbraak
Wetenschappers fabriceren veelzijdige katalysator voor polyestersynthese en -afbraak Hoe scheid je alcohol van water en krijt?
Hoe scheid je alcohol van water en krijt?  Waarom zijn kationen kleiner dan ouderionen?
Waarom zijn kationen kleiner dan ouderionen?
 Terugkerend naar de wortels van de landbouw in de strijd tegen de kever van een miljard dollar
Terugkerend naar de wortels van de landbouw in de strijd tegen de kever van een miljard dollar De effecten van revolutie en rotatie op klimaat en weer
De effecten van revolutie en rotatie op klimaat en weer Methaan uitgestoten door mensen enorm onderschat, onderzoekers vinden
Methaan uitgestoten door mensen enorm onderschat, onderzoekers vinden Uit onderzoek blijkt dat dwazen goud toch niet zo dwaas zijn
Uit onderzoek blijkt dat dwazen goud toch niet zo dwaas zijn Wat doen de delen van de hersencontrole?
Wat doen de delen van de hersencontrole?
Hoofdlijnen
- Een ingenieursgids voor het embryo
- Wat verlaagt de pH-waarde bij mensen?
- Kunnen resistente bacteriën hun resistentie verliezen?
- Hoe een eiwitfabriek te bouwen
- Wat is een celmembraan?
- Een knipperende vis onthult aanwijzingen over hoe onze voorouders uit waterland zijn geëvolueerd
- Wat betekent het aantal witte bloedcellen en differentieel?
- Onderzoek onthult enkele geheimen over hoe microben en hun genen de wereld rondreizen
- Wat is het organisme dat dood en levend is?
- Video:Het Vrijheidsbeeld ware kleuren

- Structuur van het actieve ingrediënt bismut in Pepto-Bismol onthuld
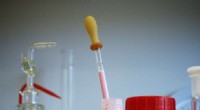
- Vitamine B7-bewakingsapparaat voor analyse van voedsel en klinische monsters
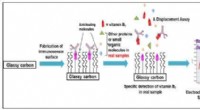
- Nieuwe methode voor het ontwerpen van metabole routes

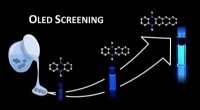
- Moleculaire bibliotheken voor organische lichtemitterende diodes
 NASA Juno maakt eerste foto's van joviaanse maan Ganymedes noordpool
NASA Juno maakt eerste foto's van joviaanse maan Ganymedes noordpool Team ontdekt dat buckyballs groter worden door verdampte koolstof te eten
Team ontdekt dat buckyballs groter worden door verdampte koolstof te eten Hoe was het verspreiden van de zeebodem om te bewijzen dat continentale drift waar was?
Hoe was het verspreiden van de zeebodem om te bewijzen dat continentale drift waar was?  Welke gassen zitten er in een ijsblokje?
Welke gassen zitten er in een ijsblokje?  Onderzoekers creëren nieuwe techniek voor het manipuleren van polarisatie van terahertz-straling
Onderzoekers creëren nieuwe techniek voor het manipuleren van polarisatie van terahertz-straling Hoeveel vloeiende gram zijn er in zeven en een halve kopjes?
Hoeveel vloeiende gram zijn er in zeven en een halve kopjes?  Welke hoeveelheid zuurstof bevat hetzelfde aantal moleculen als 36 gram water?
Welke hoeveelheid zuurstof bevat hetzelfde aantal moleculen als 36 gram water?  Blokkade in de verwijdering van cellulair afval:Wetenschappers laten zien hoe eiwitaggregaten de moleculaire balans van cellen verstoren
Blokkade in de verwijdering van cellulair afval:Wetenschappers laten zien hoe eiwitaggregaten de moleculaire balans van cellen verstoren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

