
Wetenschap
Wat is het pH -niveau van SROH2?
1. Inzicht in sterke bases
Sterke bases dissociëren volledig in water, wat betekent dat ze uit elkaar breken in hun ionen. Voor SR (OH) ₂ lijkt dit eruit:
SR (OH) ₂ (aq) → sr²⁺ (aq) + 2oH⁻ (aq)
2. POH berekenen
Aangezien SR (OH) ₂ twee hydroxide -ionen (OH⁻) voor elk molecuul produceert, heeft een oplossing van 1 m van Sr (OH) ₂ een concentratie van 2 m OH⁻ -ionen.
We kunnen de POH -formule gebruiken:
poh =-log [oh⁻]
Voor een 1 m oplossing van SR (OH) ₂:
POH =-log (2) ≈ -0.301
3. Het berekenen van pH
De relatie tussen pH en POH is:
pH + poh =14
Daarom:
pH =14 - POH ≈ 14 + 0.301 ≈ 14.301
Belangrijke opmerking:
* De werkelijke pH van een SR (OH) ₂ -oplossing hangt af van de concentratie ervan.
* Het is belangrijk op te merken dat zeer geconcentreerde oplossingen van SR (OH) ₂ pH-waarden boven 14 kunnen hebben, maar de pH-schaal is meestal beperkt tot 0-14.
Laat het me weten als je de pH van een specifieke concentratie SR (OH) ₂ wilt berekenen!
 Moleculaire feedbacklus geeft aanwijzingen hoe bloemen hun bloemblaadjes laten vallen
Moleculaire feedbacklus geeft aanwijzingen hoe bloemen hun bloemblaadjes laten vallen  Anorganische perovskietabsorbers voor gebruik in dunnefilmzonnecellen
Anorganische perovskietabsorbers voor gebruik in dunnefilmzonnecellen Uit welke 2 stoffen bestaat zout?
Uit welke 2 stoffen bestaat zout?  Slim bulkplastic reageert op licht, temperatuur en vochtigheid
Slim bulkplastic reageert op licht, temperatuur en vochtigheid Wat is Calgon-proces. Het is het proces om de hardheid van water te verwijderen?
Wat is Calgon-proces. Het is het proces om de hardheid van water te verwijderen?
 Zuid-Chili ijsberg splitst van gletsjer, bedreigt navigatie
Zuid-Chili ijsberg splitst van gletsjer, bedreigt navigatie Gericht op Trump, House stemt in met wetsvoorstel om VS in klimaatakkoord te houden
Gericht op Trump, House stemt in met wetsvoorstel om VS in klimaatakkoord te houden Nieuwe geologische vondsten uit het oosten van Fennoscandia voegen nieuwe dimensies toe aan de geschiedenis van de Europese ijstijd
Nieuwe geologische vondsten uit het oosten van Fennoscandia voegen nieuwe dimensies toe aan de geschiedenis van de Europese ijstijd Wat is een conclusie in Science Fair Project?
Wat is een conclusie in Science Fair Project?  Het droogtedilemma in Zuid-Korea ontrafelen:kunnen reservoirs een koolstofbron zijn?
Het droogtedilemma in Zuid-Korea ontrafelen:kunnen reservoirs een koolstofbron zijn?
Hoofdlijnen
- Nieuwe AI-tool legt vast hoe eiwitten zich in context gedragen
- Waarom gebruiken artsen wetenschappelijke notatie?
- De sleutelrol van enzymen in de embryonale ontwikkeling begrijpen
- Wat wordt bedoeld met cel?
- Is het waar dat de cellen van bindweefsel exact hetzelfde zijn als levercellen?
- Hoe mechanische stimuli cellulaire signalen activeren
- Hoe heet het enzym dat nieuwe nucleotiden correct aan de open DNA-streng hecht?
- Wat doen de ribosomen voor cellen?
- Wat is een reden waarom de classificatie van protisten in één koninkrijk moeilijk is?
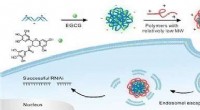
- Groene theeverbinding helpt siRNA in cellen te glippen
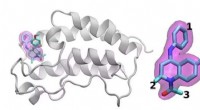
- Onderzoeksgroep gebruikt supercomputing om zich te richten op de meest veelbelovende kandidaat-geneesmiddelen uit een enorm aantal mogelijkheden
- Wetenschappers melden een nieuwe cascadereactie

- Onderzoek naar biomimicry - het bouwen van de volgende generatie aanpasbare materialen uit de natuur

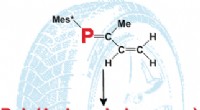
- Een chemisch functionele fosforversie van natuurlijk rubber
 Kan een donorvoucherprogramma de vertegenwoordiging in de financiering van lokale campagnes verbreden?
Kan een donorvoucherprogramma de vertegenwoordiging in de financiering van lokale campagnes verbreden? Het oplossen van de e-waste-uitdaging vereist wereldwijde actie
Het oplossen van de e-waste-uitdaging vereist wereldwijde actie De ruimte is niet het Wilde Westen:er zijn duidelijke regels voor vrede en oorlog
De ruimte is niet het Wilde Westen:er zijn duidelijke regels voor vrede en oorlog Een versnelde aanpak leidt tot de ontdekking van een nieuwe katalytische promotor die vergelijkbaar is met decennia van onderzoek
Een versnelde aanpak leidt tot de ontdekking van een nieuwe katalytische promotor die vergelijkbaar is met decennia van onderzoek  Hoeveel van het heelal bestaat uit waterstof?
Hoeveel van het heelal bestaat uit waterstof?  FoodTracker:een door AI aangedreven mobiele applicatie voor voedseldetectie
FoodTracker:een door AI aangedreven mobiele applicatie voor voedseldetectie De Archeïsche Oceaan als ideale broedplaats voor leven
De Archeïsche Oceaan als ideale broedplaats voor leven Welke eilanden worden gevonden in de Caribische Zee?
Welke eilanden worden gevonden in de Caribische Zee?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

