
Wetenschap
Hoe zijn de termen molaire massa en atoom hetzelfde?
Atomische massa:
* Verwijst naar de massa van een enkel atoom van een element.
* Gemeten in atomaire massa -eenheden (AMU).
* Vertegenwoordigt de gemiddelde massa van alle isotopen van dat element, rekening houdend met hun relatieve overvloed.
Molaire massa:
* Verwijst naar de massa van één mol van een stof (element of verbinding).
* Gemeten in gram per mol (g/mol).
* Numeriek equivalent aan de atomaire massa van het element, maar met de eenheden veranderd in grammen per mol.
Relatie:
De belangrijkste verbinding is dat de numerieke waarde van de atomaire massa van een element hetzelfde is als de numerieke waarde van zijn molaire massa.
* Bijvoorbeeld, de atoommassa van koolstof is 12.01 AMU en de molaire massa is 12,01 g/mol.
Sleutelverschil:
Het belangrijkste verschil is de meeteenheid . Atomische massa wordt gemeten in AMU, een zeer kleine eenheid, terwijl molaire massa wordt gemeten in gram per mol, wat een meer praktische eenheid is voor dagelijks gebruik.
Samenvattend:
* Atomische massa is de massa van een enkel atoom.
* Molaire massa is de massa van één mol van een stof.
* Beide hebben dezelfde numerieke waarde, maar verschillende eenheden.
 Eiwitvoeding voor cellen en organismen:kunnen we het gebruiken om ziekten te behandelen?
Eiwitvoeding voor cellen en organismen:kunnen we het gebruiken om ziekten te behandelen? Synthetische biologen hacken bacteriële sensoren
Synthetische biologen hacken bacteriële sensoren Het mysterie van het moeilijkste materiaal van de natuur kraken
Het mysterie van het moeilijkste materiaal van de natuur kraken Welke elementen hebben de kleinste atoomstraal broom, zwavel, chloor of selenium?
Welke elementen hebben de kleinste atoomstraal broom, zwavel, chloor of selenium?  Welke stof wordt gevonden in de menselijke huid die reageert met ninhydrin dat resulteert op vlekken?
Welke stof wordt gevonden in de menselijke huid die reageert met ninhydrin dat resulteert op vlekken?
 Luchtvervuiling veroorzaakt door maïsproductie verhoogt sterftecijfer in VS
Luchtvervuiling veroorzaakt door maïsproductie verhoogt sterftecijfer in VS Hoe ijsnaalden patronen van stenen weven in bevroren landschappen
Hoe ijsnaalden patronen van stenen weven in bevroren landschappen Koolstofafvang en -conversie mogen niet afhankelijk zijn van zeldzame metalen
Koolstofafvang en -conversie mogen niet afhankelijk zijn van zeldzame metalen Heliumballonnen bieden goedkope vluchten naar de stratosfeer
Heliumballonnen bieden goedkope vluchten naar de stratosfeer Zaailingen staan voor zware strijd met klimaatverandering
Zaailingen staan voor zware strijd met klimaatverandering
Hoofdlijnen
- Wat is nodig voor de glycolyse om te beginnen?
- Wanneer ontstonden genetische variaties die ons menselijk maken?
- Onderzoekers laten zien hoe deep learning het onderzoek naar neurale degeneratie kan bevorderen
- Omdat het kan, betekent dit ook dat we moeten? De ethiek van genetisch gemodificeerd voedsel
- Biodiversiteit behouden of genetische diversiteit plunderen? Wat doet het fokken in gevangenschap met de vispopulaties?
- Wat is de medische term die niet betekent dat niet -ranselcel niet is?
- Het 'lees-schrijf'-mechanisme van de cel:Onderzoekers ontdekken hoe instructies voor genexpressie worden doorgegeven
- Wat is de meester -hormonale klier?
- Hoe verander je de celtheorie in de wet?
- Chaperones bereiden eiwitten gewoon voor om zelf te vouwen
- Natuurlijke blauwe voedselkleuring krijgt een milieuvriendelijke productieboost

- Spinazie gebruikt in neutronenstudies zou het geheim kunnen ontrafelen voor een sterkere plantengroei

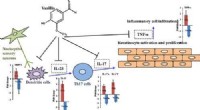
- Psoriasis voorkomen met vanilline
- Nieuwe MD-simulatie werpt licht op het mysterie van de structuur van gehydrateerde elektronen

 Onderzoek toont aan hoe klimaatverandering de impact van invasieve planten kan verergeren
Onderzoek toont aan hoe klimaatverandering de impact van invasieve planten kan verergeren  De chaos in lichtbronnen onder controle brengen
De chaos in lichtbronnen onder controle brengen Vormt hetzelfde proces alle soorten sedimentair gesteente?
Vormt hetzelfde proces alle soorten sedimentair gesteente?  Welke factoren zijn belangrijk bij het beoordelen hoe nuttig een energiebron voor ons is?
Welke factoren zijn belangrijk bij het beoordelen hoe nuttig een energiebron voor ons is?  Tech-leider van American Airlines praat over storingen, hackers
Tech-leider van American Airlines praat over storingen, hackers Hebben we het piekverkeer bereikt?
Hebben we het piekverkeer bereikt?  In een eerste, elektrische auto's verkopen beter dan traditionele in Noorwegen
In een eerste, elektrische auto's verkopen beter dan traditionele in Noorwegen Wat is de reactie tussen alcoholisch KOH en alkylhalogenide?
Wat is de reactie tussen alcoholisch KOH en alkylhalogenide?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

