
Wetenschap
Wat is de kathode in een elektrochemische cel?
Hier is een uitsplitsing:
* reductie: Het proces van het verkrijgen van elektronen.
* oxidatie: Het proces van het verliezen van elektronen.
* kathode: De elektrode waar reductie optreedt.
* anode: De elektrode waar oxidatie optreedt.
Belangrijke punten om te onthouden:
* elektronen stromen van de anode naar de kathode.
* In een galvanische (voltaïsche) cel is de kathode de positieve elektrode. Dit komt omdat elektronen er vanuit de anode naar toe stromen.
* In een elektrolytische cel is de kathode de negatieve elektrode. Dit komt omdat een externe stroombron elektronen dwingt om ernaar te stromen.
Voorbeeld:
In een eenvoudige batterij is de kathode vaak gemaakt van een metaalachtig koper. Tijdens de werking van de batterij krijgen koperionen van de elektrolytoplossing elektronen bij de kathode, waardoor ze worden gereduceerd tot koperen metaal. Dit wordt weergegeven door de volgende halve reactie:
Cu²⁺ (aq) + 2e⁻ → cu (s)
 Is sucrose een zuivere stof of mengsel?
Is sucrose een zuivere stof of mengsel?  Duizenden moleculen scannen tegen een ongrijpbaar kankerdoelwit
Duizenden moleculen scannen tegen een ongrijpbaar kankerdoelwit Druppeltjes die naar oplossing zwemmen, kunnen vloeibare microbots inspireren
Druppeltjes die naar oplossing zwemmen, kunnen vloeibare microbots inspireren  Welk element B C P zal, indien gecombineerd met jodium, de grootste aantrekkingskracht op elektronen hebben?
Welk element B C P zal, indien gecombineerd met jodium, de grootste aantrekkingskracht op elektronen hebben?  Onderzoekers observeren een abnormaal stress-geheugeneffect dat stress-ontspanning in glas tegenhoudt
Onderzoekers observeren een abnormaal stress-geheugeneffect dat stress-ontspanning in glas tegenhoudt
 Adaptief beheer van bodembehoud is essentieel voor het verbeteren van de waterkwaliteit, uit onderzoek blijkt
Adaptief beheer van bodembehoud is essentieel voor het verbeteren van de waterkwaliteit, uit onderzoek blijkt Oliekranen dichtdraaien? Noorwegen verscheurd tussen klimaat en cash
Oliekranen dichtdraaien? Noorwegen verscheurd tussen klimaat en cash Internationaal onderzoek onderzoekt de oorzaak van de migratie van herten
Internationaal onderzoek onderzoekt de oorzaak van de migratie van herten  Als het om water gaat, denk globaal
Als het om water gaat, denk globaal Het vertragen van de klimaatverandering kan het drogen in de subtropen omkeren
Het vertragen van de klimaatverandering kan het drogen in de subtropen omkeren
Hoofdlijnen
- Wat is Abiotic in het ecosysteem?
- Netwerkassemblage door celdeling:hoe zenuwcellen in de hersenen verbinding maken tijdens de ontwikkeling
- Hoe lijken mitochondriën en chloroplasten op bacteriën?
- Welke microscopisch kleine bacteriën veranderen melk in yoghurt?
- Wetenschappers ontcijferen mechanismen die ten grondslag liggen aan de biologie van veroudering
- Wat betekent M in de wetenschap?
- Wat zou de impact zijn op planten- en dierlijke cellen als water niet bestaat?
- Kunnen we een echt Jurassic Park creëren?
- Wat zijn de twee belangrijke variabelen in een onderzoekstitel?
- Nieuwe technologie zet biomassa om in steenkool

- Chirale krabben

- Hoe drie mutaties samenwerken om nieuwe SARS-CoV-2-varianten te stimuleren
- Wetenschappers produceren eerste open source all-atom-modellen van COVID-19 spike-eiwit

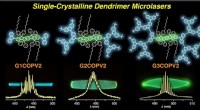
- Dendrimers hebben eindelijk wat nodig is om door te breken in de laserscene
 Wat zijn de 4 hoofdonderdelen van een virus?
Wat zijn de 4 hoofdonderdelen van een virus?  Beoordeling van de lock-outwetten in Sydney benadrukt de cruciale rol van transparante gegevensanalyse
Beoordeling van de lock-outwetten in Sydney benadrukt de cruciale rol van transparante gegevensanalyse Waarom geven mensen er de voorkeur aan om privé te paren?
Waarom geven mensen er de voorkeur aan om privé te paren?  De welzijnsparadox:mensen worden rijker, maar niet meer tevreden
De welzijnsparadox:mensen worden rijker, maar niet meer tevreden Onderzoek toont aan hoe luchtvervuiling de verwachte toename van de regenval heeft gecompenseerd
Onderzoek toont aan hoe luchtvervuiling de verwachte toename van de regenval heeft gecompenseerd  Ingenieurs zappen en maken onderwater slimme lijm los
Ingenieurs zappen en maken onderwater slimme lijm los Ontmoet de boeren van de toekomst:Robots
Ontmoet de boeren van de toekomst:Robots Hubble beeldt een complex galactisch trio in
Hubble beeldt een complex galactisch trio in
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

