
Wetenschap
Hoe verklaar je de eigenaardigheid op het zoutgehalte van zeewater en op dezelfde manier voor hardheid water?
zoutgehalte van zeewater:
eigenaardigheid: Zeewater is zout, met een gemiddeld zoutgehalte van ongeveer 3,5%. Dit betekent dat voor elke 1000 gram zeewater 35 gram opgelost zouten zijn.
Verklaring:
* verwering en erosie: Rotsen op het land worden constant verweerd en geërodeerd door regen, wind en rivieren. Deze processen geven opgeloste mineralen en zouten vrij, die in de oceaan worden gedragen.
* Hydrothermische ventilatieopeningen: Vulkanen onder water en hydrothermische ventilatieopeningen geven opgeloste mineralen en zouten in de oceaan vrij.
* vulkaanuitbarstingen: Vulkanische uitbarstingen kunnen ook aanzienlijke hoeveelheden zouten in de atmosfeer afgeven, die uiteindelijk als regen in de oceaan vallen.
* Verdamping en neerslag: Terwijl zeewater verdampt, blijven de opgeloste zouten achter, waardoor het zoutgehalte van het resterende water wordt vergroot. Dit proces wordt echter in evenwicht gebracht door neerslag, wat de zoutconcentratie verwijdt.
* Balans van ingangen en uitgangen: Het zoutgehalte van zeewater wordt gehandhaafd door een evenwicht tussen de input van zouten en de uitgangen, zoals de vorming van zeezoutafzettingen en de verwijdering van zouten door organismen.
Factoren die het zoutgehalte beïnvloeden:
* Latitude: Het zoutgehalte is over het algemeen hoger in warmere, drogere regio's als gevolg van verhoogde verdamping.
* Locatie: Het zoutgehalte varieert afhankelijk van de locatie, beïnvloed door factoren zoals rivierinstroom, de nabijheid van ijsmelt en oceaanstromingen.
* diepte: Zoutgehalte kan variëren met diepte, waarbij de oppervlaktelaag meestal minder zout is dan diepere lagen.
Hardheid van water:
eigenaardigheid: Hard water bevat hoge concentraties van opgeloste mineralen, voornamelijk calcium en magnesium.
Verklaring:
* Geologische vorming: De reis van het water door de grond, vooral door kalksteen- en dolomietformaties, lost deze mineralen op.
* verwering en ontbinding: Regenwater is enigszins zuur, waardoor het calcium en magnesium van rotsen kan oplossen.
* menselijke activiteiten: Industriële processen, zoals mijnbouw en landbouw, kunnen bijdragen aan de hardheid van water door mineralen in de watervoorziening vrij te geven.
Soorten hardheid:
* Tijdelijke hardheid: Veroorzaakt door opgeloste calcium- en magnesiumbicarbonaten. Het kan worden verwijderd door het water te koken.
* Permanente hardheid: Veroorzaakt door opgeloste calcium- en magnesiumsulfaten en chloriden. Koken verwijdert het niet.
gevolgen van hard water:
* Schaalvorming: Hard water kan schaalafzettingen vormen in leidingen en apparaten, waardoor de efficiëntie wordt verminderd en mogelijk schade veroorzaakt.
* Soap Scum: Hard water reageert met zeep om een wit, zeepachtige residu te vormen.
* droge huid en haar: Hard water kan natuurlijke oliën van huid en haar ontdoen, waardoor ze droog en bros aanvoelen.
Zowel zoutgehalte als waterhardheid zijn belangrijke factoren om in verschillende contexten te overwegen, van menselijke gezondheid en landbouw tot industriële processen en milieuduurzaamheid. Inzicht in de eigenaardigheden en oorsprong van deze eigenschappen helpt ons om waterbronnen effectief te beheren en gerelateerde uitdagingen aan te gaan.
 Is goud een samengesteld element homo of hetero?
Is goud een samengesteld element homo of hetero?  Waarom verandert de kleur van kopersulfaat als je er een ijzeren spijker in doopt?
Waarom verandert de kleur van kopersulfaat als je er een ijzeren spijker in doopt?  Interdisciplinair team ontwerpt gasstroomcel om katalytisch gedrag te analyseren
Interdisciplinair team ontwerpt gasstroomcel om katalytisch gedrag te analyseren Wat is de groep van het periodiek systeem?
Wat is de groep van het periodiek systeem?  Onderzoekers laten zien dat materialen vanzelf sterker worden wanneer ze met zeer hoge snelheid worden geraakt
Onderzoekers laten zien dat materialen vanzelf sterker worden wanneer ze met zeer hoge snelheid worden geraakt
 Vuile ramen kunnen giftige stoffen bevatten
Vuile ramen kunnen giftige stoffen bevatten Symbiotische relaties voor neushoorns
Symbiotische relaties voor neushoorns We hebben een AI-tool gebouwd om prioriteiten te stellen voor natuurbehoud in Madagaskar:wat we hebben gevonden
We hebben een AI-tool gebouwd om prioriteiten te stellen voor natuurbehoud in Madagaskar:wat we hebben gevonden  Don en Hilary stormen in de buurt van de VS
Don en Hilary stormen in de buurt van de VS Sociaal-economisch onderzoek kijkt naar het vergroten van de betrouwbaarheid van het Panamakanaal
Sociaal-economisch onderzoek kijkt naar het vergroten van de betrouwbaarheid van het Panamakanaal
Hoofdlijnen
- Antibioticavervuiling verstoort het darmmicrobioom en blokkeert het geheugen van waterslakken, zo blijkt uit onderzoek
- Welke rol speelt de zuurstof in cellulaire ademhaling?
- Stopt mitochondriën niet meer functioneren in een eencellig organisme dat wordt blootgesteld aan verontreinigende stoffen duidt op het orgaansysteem?
- Wat is er nodig bij een wetenschappelijke methode?
- Lasers en een aangepaste microscoop tonen het gensplitsingsproces in realtime
- Het visfeest is in wezen een benzinestation en trekt zeeleeuwen naar Pier 39 in aantallen die in 15 jaar niet meer zijn gezien
- Waarom lachen mensen als ze gekieteld worden?
- Wat zijn biologisch gebruik?
- Hoe vampieren werken
- Bier brouwen dat langer vers smaakt

- Door de bodem kijken kan boeren helpen om toekomstige droogtes het hoofd te bieden

- Baanbrekende nieuwe herbruikbare lijm werkt onder water

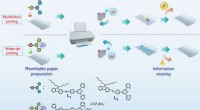
- Speciaal papier kan meerdere keren worden gewist en bedrukt
- Chemici ontdekken nieuwe kenmerken om cystische fibrose bij zuigelingen eerder te identificeren

 Emissies van fossiele brandstoffen volgen met koolstof-14
Emissies van fossiele brandstoffen volgen met koolstof-14 Hoe kom je op de wetenschapsquiz 100 procent?
Hoe kom je op de wetenschapsquiz 100 procent?  Het verschil tussen craniologie en frenologie
Het verschil tussen craniologie en frenologie
Craniologie en frenologie zijn beide praktijken die de conformatie van de menselijke schedel onderzoeken; echter, de twee zijn heel verschillend. Craniologie is de studie van verschillen in vorm, groott
 Nieuwe wiskundige methode laat zien hoe klimaatverandering leidde tot de ondergang van de oude beschaving
Nieuwe wiskundige methode laat zien hoe klimaatverandering leidde tot de ondergang van de oude beschaving Het effect van PH in rivierwater
Het effect van PH in rivierwater  Meer preventie-inspanningen nodig om het groeiende risico op toekomstige bosbranden in te dammen
Meer preventie-inspanningen nodig om het groeiende risico op toekomstige bosbranden in te dammen Kan een Neanderthaler mediteren?
Kan een Neanderthaler mediteren? Wat is informele observatie?
Wat is informele observatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

