
Wetenschap
Waarom isotopen van een element met minder neutronen hebben lagere dichtheden en smeltende kookpunten?
1. Nucleaire massa en dichtheid:
* zwaardere isotopen: Isotopen met meer neutronen hebben een grotere nucleaire massa. Dit verhoogt direct de totale massa van het atoom. Voor een bepaald volume betekent een hogere massa een hogere dichtheid.
* Echter: De verandering in dichtheid als gevolg van de extra neutronen is meestal klein, vooral in vergelijking met andere factoren die de dichtheid beïnvloeden, zoals atoompakking en interatomische krachten.
2. Interatomische krachten:
* isotopen en binding: Het aantal neutronen heeft niet direct invloed op de sterkte van chemische bindingen tussen atomen. Dit wordt voornamelijk bepaald door het aantal protonen (dat het element definieert) en de elektronenconfiguratie.
* Echter: Isotopen met minder neutronen kunnen iets zwakkere interatomische krachten hebben. Dit komt omdat:
* Kleinere nucleaire grootte: Minder neutronen kunnen leiden tot een iets kleinere kern, wat resulteert in een iets kleinere atoomradius. Dit kan de aantrekkelijke krachten tussen atomen verzwakken.
* trillingsfrequenties: Isotopen met verschillende massa's zullen trillen op verschillende frequenties. Deze verschillen kunnen de sterkte van interatomische krachten beïnvloeden.
3. Smelten en kookpunten:
* Interatomische krachtcorrelatie: Smelten en kookpunten worden grotendeels bepaald door de sterkte van interatomische krachten die de stof bij elkaar houden. Zwakkere krachten betekenen lagere smelt- en kookpunten.
* isotoopvariatie: De subtiele veranderingen in interatomische krachten als gevolg van neutronenaantal kunnen soms leiden tot kleine variaties in smelten en kookpunten. Deze variaties zijn echter vaak relatief klein in vergelijking met het totale bereik van smelt- en kookpunten over verschillende elementen.
4. Andere factoren:
* kwantumeffecten: In sommige gevallen, vooral voor lichtere elementen, kunnen kwantumeffecten een rol spelen in de verschillen tussen isotopen. Deze effecten kunnen de trillingsfrequenties en de algehele energieniveaus van de atomen beïnvloeden.
Samenvattend:
* Isotopen met minder neutronen zijn inderdaad iets minder dicht vanwege hun lagere massa, maar het effect is vaak klein.
* De impact op smelten en kookpunten is nog minder voorspelbaar. Terwijl zwakkere interatomische krachten als gevolg van minder neutronen deze punten kunnen verlagen, spelen andere factoren zoals het specifieke element en de bindingseigenschappen ervan een belangrijkere rol.
Het is belangrijk op te merken dat de relatie tussen neutronennummer en dichtheid/smelten/kookpunt niet altijd consistent is. Er zijn uitzonderingen en elke isotoop moet afzonderlijk worden overwogen.
 Het Euraziatische continent onthoudt en versterkt koude golven naarmate het noordpoolgebied opwarmt
Het Euraziatische continent onthoudt en versterkt koude golven naarmate het noordpoolgebied opwarmt Deze Amerikaanse energiecentrale laat zien waarom steenkool sterft,
Deze Amerikaanse energiecentrale laat zien waarom steenkool sterft,  Wat milieukwesties betreft, is de kloof tussen stad en land in Zwitserland kleiner dan vaak wordt aangenomen
Wat milieukwesties betreft, is de kloof tussen stad en land in Zwitserland kleiner dan vaak wordt aangenomen NASA-NOAA-satelliet vangt vorming van tropische cycloon Lili
NASA-NOAA-satelliet vangt vorming van tropische cycloon Lili Hoe het zien van lijken de levensduur van vliegen verkort
Hoe het zien van lijken de levensduur van vliegen verkort
Hoofdlijnen
- Wat is het controlecentrum van de cel dat nodig is voor deling en het leven?
- Hoe wordt ATP gebruikt?
- Hoe door klimaatverandering veroorzaakte stress de hormonen van vissen verandert – met enorme gevolgen voor de voortplanting
- Wilde vogels:oplevende kalkoenen sparren met menselijke buren
- Hoe het placebo-effect werkt
- Vangstvissen kan temperatuurpieken veroorzaken bij haaien
- Wat is Diane definitie van wetenschap?
- Wat zijn de onderdelen en functie van gistcel?
- Noordelijke maïsbladziekte-genen geïdentificeerd in nieuwe studie
- Wetenschappers ontdekken een nieuw complex europiumhydride

- Quasikristalhelder:materiaal onthult unieke verschuivende oppervlaktestructuur onder microscoop
- Hoe water het substraat in het enzym helpt

- Kleine molecule transporteert ijzer in muizen, menselijke cellen om bepaalde vormen van bloedarmoede te behandelen
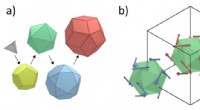
- Nieuw raamwerk past machine learning toe op atomistische modellering

 Hoe heet de arbeid die in een machine gaat?
Hoe heet de arbeid die in een machine gaat?  Muzikale sensor geeft aan dat slecht medicijn een valse noot speelt
Muzikale sensor geeft aan dat slecht medicijn een valse noot speelt De toekomst van hernieuwbare energie verlichten
De toekomst van hernieuwbare energie verlichten Welke bedrijven gaan in 2022 naar de beurs? Bijna geen tot nu toe
Welke bedrijven gaan in 2022 naar de beurs? Bijna geen tot nu toe Zijn groene huishoudelijke consumentenproducten minder giftig dan traditionele producten?
Zijn groene huishoudelijke consumentenproducten minder giftig dan traditionele producten? Trage Covid-vaccinatie kost de wereldeconomie $ 2,3 tn:studie
Trage Covid-vaccinatie kost de wereldeconomie $ 2,3 tn:studie De wetenschap van straatprotesten opvoeren
De wetenschap van straatprotesten opvoeren 10 mythes over bliksem
10 mythes over bliksem
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

