
Wetenschap
Waarom is natrium minder reactief dan kalium?
Een andere manier om hiernaar te kijken is dat het kaliumatoom kleiner is dan het natriumatoom. De kleinere omvang van het kaliumatoom betekent dat de buitenste elektronen steviger door de kern worden vastgehouden, waardoor het minder waarschijnlijk is dat ze worden verwijderd en daardoor kalium minder reactief wordt.
Bovendien heeft kalium een lagere ionisatie-energie dan natrium. Ionisatie-energie is de energie die nodig is om een elektron uit een atoom te verwijderen. De lagere ionisatie-energie van kalium betekent dat kalium gemakkelijker een elektron kan verliezen en daardoor kan worden geoxideerd, waardoor het reactiever wordt.
Concluderend:het feit dat natrium een grotere atoomstraal, een hogere ionisatie-energie en een minder effectieve nucleaire lading heeft dan kalium, maakt het minder reactief dan kalium.
 Uranium ter vervanging van plastic? Doorbraak in de chemie kan de weg vrijmaken voor nieuwe materialen
Uranium ter vervanging van plastic? Doorbraak in de chemie kan de weg vrijmaken voor nieuwe materialen Hydrogel geneest zonder toevoegingen
Hydrogel geneest zonder toevoegingen Studie analyseert de sleutels tot fragmentatie van metalen materialen
Studie analyseert de sleutels tot fragmentatie van metalen materialen Rationeel ontwerpen van hiërarchische zeolieten voor betere diffusie en katalysatorefficiëntie
Rationeel ontwerpen van hiërarchische zeolieten voor betere diffusie en katalysatorefficiëntie Wat is de meest voorkomende natriumverbinding?
Wat is de meest voorkomende natriumverbinding?
 Filosoof pakt wereldwijde aantasting van het milieu frontaal aan
Filosoof pakt wereldwijde aantasting van het milieu frontaal aan De regering van Biden stelt voor het recht van Californië te herstellen om regels voor autovervuiling vast te stellen
De regering van Biden stelt voor het recht van Californië te herstellen om regels voor autovervuiling vast te stellen Welk Biome heeft de minste biodiversiteit?
Welk Biome heeft de minste biodiversiteit?  Video:Beeldmateriaal laat zien hoe drones het behoud van schildpadden kunnen stimuleren
Video:Beeldmateriaal laat zien hoe drones het behoud van schildpadden kunnen stimuleren  Indicatoren wijzen op ergere overstromingen van de Grote Meren dan in 2017
Indicatoren wijzen op ergere overstromingen van de Grote Meren dan in 2017
Hoofdlijnen
- Dode vissen en depressies aan de oevers van de Oder
- Wat is de medische term voor weefselceldood in de huid?
- Onderzoekers bewerken genen om COVID-19 te voorkomen en te behandelen in het laboratorium. Werkt het bij mensen?
- Hoe een stedelijke vleermuis verschilt van een landelijke vleermuis
- Het idee testen dat milieu-uitdagingen de evolutie van grotere hersenen stimuleren
- Wetenschappers tonen moleculaire basis voor mieren die als lijfwachten voor planten fungeren
- Stijgende kwikniveaus kunnen bijdragen aan de afnemende populaties Steller-zeeleeuwen
- Wat is de juiste volgorde voor de volgorde van de meiose?
- Onderzoekers tonen bewijs van 'geheugen' in cellen en moleculen
- Serendipity verbreedt de mogelijkheden voor het maken van grafiet

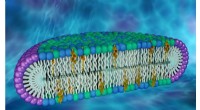
- Nieuw celmembraanmodel kan de sleutel zijn tot het ontdekken van nieuwe eiwiteigenschappen
- Nieuwe theorieën en materialen helpen de overgang naar schone energie

- Nieuwe materialen kunnen wondgenezing stimuleren door gebruik te maken van natuurlijke genezingsmethoden

- Dynamische afbeeldingen tonen ruitvormige protease in actie
 Wat gebeurt er met een bal die recht naar beneden wordt gegooid vanaf de brug en een versnelling zou hebben?
Wat gebeurt er met een bal die recht naar beneden wordt gegooid vanaf de brug en een versnelling zou hebben?  Mannelijke en vrouwelijke brandweerlieden hebben verschillende problemen met beschermende pakken
Mannelijke en vrouwelijke brandweerlieden hebben verschillende problemen met beschermende pakken Wat zijn de verschillende soorten land?
Wat zijn de verschillende soorten land?  Model toont Welshe taal die niet met uitsterven wordt bedreigd, maar te reo Māori is op weg naar buiten
Model toont Welshe taal die niet met uitsterven wordt bedreigd, maar te reo Māori is op weg naar buiten De inspanningen om de CO2-uitstoot in Californië te verminderen, kunnen worden gedwarsboomd door de klimaatverandering zelf
De inspanningen om de CO2-uitstoot in Californië te verminderen, kunnen worden gedwarsboomd door de klimaatverandering zelf Oudere en armere gemeenschappen worden achtergelaten door de achteruitgang van contant geld
Oudere en armere gemeenschappen worden achtergelaten door de achteruitgang van contant geld Hoe biometrie werkt
Hoe biometrie werkt  Delhi houdt adem in terwijl brandende boerderijen het vervuilingsseizoen inluiden
Delhi houdt adem in terwijl brandende boerderijen het vervuilingsseizoen inluiden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

