
Wetenschap
Hoeveel mol ammoniakgas ontstaat bij de reactie van 3 mol stikstof met een overmaat waterstof N2 H2 ---- NH3?
De uitgebalanceerde chemische vergelijking voor de reactie tussen stikstof en waterstof om ammoniak te produceren is:
$$N_2 + 3H_2 \pijl naar rechts 2NH_3$$
Volgens de stoichiometrie van de vergelijking reageert 1 mol stikstof met 3 mol waterstof om 2 mol ammoniak te produceren. Als er dus 3 mol stikstof wordt gebruikt bij de reactie met een overmaat aan waterstof, kan het aantal geproduceerde mol ammoniak als volgt worden berekend:
Mol ammoniak =(3 mol stikstof) × (2 mol ammoniak / 1 mol stikstof) =6 mol ammoniak
Daarom zal 3 mol stikstof 6 mol ammoniakgas produceren wanneer het reageert met een overmaat waterstof.
 'Otterly schattig'?:De vraag naar schattige selfies brengt dieren in gevaar
'Otterly schattig'?:De vraag naar schattige selfies brengt dieren in gevaar  Wat is de meest giftige spin voor mensen?
Wat is de meest giftige spin voor mensen?  Vliegend laboratorium onthult cruciale doelen voor het behoud van tropische bossen in Borneo
Vliegend laboratorium onthult cruciale doelen voor het behoud van tropische bossen in Borneo De zeer eenzame seismometer:een slapende aardbevingsbewakingsprogramma's laatste overblijfselen
De zeer eenzame seismometer:een slapende aardbevingsbewakingsprogramma's laatste overblijfselen Sla laat zien hoe je met olie doordrenkte grond kunt herstellen
Sla laat zien hoe je met olie doordrenkte grond kunt herstellen
Hoofdlijnen
- Wat draagt het meest bij aan de vervuiling?
- Wetenschappers onthullen waarom buikwantsen zo goed door je darmen kunnen zwemmen
- Wat maakt een dominant allel anders dan een recessief allel?
- Verschillende Agar-platen
- Transporteert het gladde er eiwitten?
- Welke wetenschapper stelde dat alle organismen evolueerden naar perfectie en complexiteit?
- Waarom stemmen mensen? Genetische variatie in politieke participatie
- Hoe erfelijke ziekten werken
- Hoeveel enzymen zitten er in één cel?
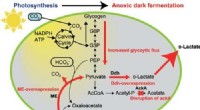
- Methode levert een hoog percentage D-lactaat op met behulp van cyanobacteriën, kan een revolutie teweegbrengen in de productie van bioplastic
- Waterstofeffecten in metaal observeren

- Plastic afval omzetten in waterstofgas en koolstofnanobuisjes

- Wetenschappers bevorderen de creatie van kunstmatige lymfeklieren om kanker te bestrijden, andere ziekten
- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

 Het leven zou kunnen overleven, en gedijen, in een waterstofwereld:studie
Het leven zou kunnen overleven, en gedijen, in een waterstofwereld:studie Wetenschappers ontdekken dat omdraaiende lagen in heterostructuren veranderingen in hun eigenschappen veroorzaken
Wetenschappers ontdekken dat omdraaiende lagen in heterostructuren veranderingen in hun eigenschappen veroorzaken  Hoe het ruwe geboortecijfer te berekenen
Hoe het ruwe geboortecijfer te berekenen Bosbranden bereiken Melbourne terwijl hittegolffans Australië laaien
Bosbranden bereiken Melbourne terwijl hittegolffans Australië laaien Hoe we onze planeet koel kunnen houden, zelfs als het gebruik van airconditioning stijgt
Hoe we onze planeet koel kunnen houden, zelfs als het gebruik van airconditioning stijgt Onderzoek toont aan dat het moeilijk is om bewijs van leven op Mars te vinden
Onderzoek toont aan dat het moeilijk is om bewijs van leven op Mars te vinden Hoeveel brandstof heeft de zon verbruikt?
Hoeveel brandstof heeft de zon verbruikt?  Afbeelding:Hera-logo aan boord van ISS
Afbeelding:Hera-logo aan boord van ISS
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

