
Wetenschap
Wat zijn de eigenschappen van fluor?
* Symbool: F
* Atoomnummer: 9
* Atoomgewicht: 18.9984032
* Elektronenconfiguratie: 1s2 2s2 2p5
* Valentie-elektronen: 7
* Oxidatietoestanden: -1, 0, +1, +2, +3, +4, +5, +6, +7
* Elektronegativiteit: 4,0 (Pauling-schaal)
* Ionisatie-energie: 1680 kJ/mol (eerste), 3374 kJ/mol (tweede), 6050 kJ/mol (derde), 8408 kJ/mol (vierde)
* Covalente straal: 71 uur
* Ionische straal: 133 uur (V-)
* Smeltpunt: −219,62 °C
* Kookpunt: −188,12 °C
* Dichtheid (bij 25 °C): 1,696 g/l
* Kleur: Lichtgeel
Fysieke eigenschappen
Fluor is bij kamertemperatuur een lichtgeel diatomisch gas. Het is de lichtste van de halogenen en het meest reactieve element in het periodiek systeem. Fluorgas is corrosief, giftig en kan met bepaalde materialen explosieve mengsels vormen.
Chemische eigenschappen
Fluor is het meest reactieve van alle elementen en kan reageren met vrijwel elk ander element, behalve de edelgassen. Fluor reageert met alle metalen om fluoriden te vormen, en het reageert met de meeste niet-metalen om covalente verbindingen te vormen. Fluor staat ook bekend om zijn vermogen om stabiele polyatomaire ionen te vormen, zoals fluoriden (F-), bifluoriden (HF2-) en trifluoriden (F3-).
Gebruik
Fluor wordt gebruikt in verschillende toepassingen, waaronder:
* Productie van uraniumhexafluoride (UF6), dat wordt gebruikt bij de verrijking van uranium voor kernbrandstof en wapens.
* Productie van fluorwaterstofzuur (HF), dat wordt gebruikt in de halfgeleiderindustrie, het etsen van glas en het reinigen van metaal.
* Productie van gefluoreerde polymeren, die worden gebruikt in een verscheidenheid aan toepassingen, zoals kookgerei met antiaanbaklaag, elektrische isolatie en medische apparaten.
* Fluoridering van drinkwater, wat tandbederf helpt voorkomen.
Gevaren
Fluor is een gevaarlijke stof die ernstige gezondheidsproblemen kan veroorzaken, waaronder:
* Brandwonden: Fluorgas kan ernstige brandwonden aan de huid en ogen veroorzaken.
* Ademhalingsproblemen: Inademing van fluorgas kan ademhalingsproblemen veroorzaken, zoals bronchitis en longontsteking.
* Botschade: Fluor kan botten en tanden beschadigen, wat kan leiden tot aandoeningen zoals osteoporose en fluorose.
* Kanker: Fluor is in verband gebracht met een verhoogd risico op bepaalde soorten kanker, zoals longkanker en blaaskanker.
Voorzorgsmaatregelen
Ter bescherming tegen de gevaren van fluor moeten werknemers de volgende voorzorgsmaatregelen nemen:
* Draag persoonlijke beschermingsmiddelen, zoals handschoenen, een veiligheidsbril en een gasmasker.
* Werk in een goed geventileerde ruimte.
* Bewaar fluorgas in een veilige container op een koele, droge plaats.
* Volg alle veiligheidsprocedures bij het werken met fluor.
 Vloeibaar water is meer dan alleen waterstof-zuurstofmoleculen
Vloeibaar water is meer dan alleen waterstof-zuurstofmoleculen Meertraps vervormingsproces in legeringen met hoge entropie bij ultralage temperaturen onthuld
Meertraps vervormingsproces in legeringen met hoge entropie bij ultralage temperaturen onthuld Kankercellen targeten door elektrische stromen te meten
Kankercellen targeten door elektrische stromen te meten Waarom is de oppervlaktespanning van water hoger dan die van methaan?
Waarom is de oppervlaktespanning van water hoger dan die van methaan?  Algen als microscopisch kleine bioraffinaderijen
Algen als microscopisch kleine bioraffinaderijen
 Maskers en handschoenen redden levens en veroorzaken vervuiling
Maskers en handschoenen redden levens en veroorzaken vervuiling Water omringt de stad Mississippi terwijl rivieren over het zuiden rijzen
Water omringt de stad Mississippi terwijl rivieren over het zuiden rijzen Hoe Pileated spechten aan te trekken met Suet aan de zijkant van een boom
Hoe Pileated spechten aan te trekken met Suet aan de zijkant van een boom  Bosbranden domineren in toenemende mate de koolstofemissies in de Amazone tijdens droogtes
Bosbranden domineren in toenemende mate de koolstofemissies in de Amazone tijdens droogtes wat beschrijft de klimaatverandering het beste?
wat beschrijft de klimaatverandering het beste?
Hoofdlijnen
- Verbetering van de detectie van antilichamen tegen het Afrikaanse varkenspestvirus in serum
- Wat doen zowel zaden als planten voordat ze beginnen te groeien?
- De kleur van de evolutie:hoe één vis twee werd
- Man of vrouw? Bij vliegen kunnen sommige cellen het niet zien
- Onderzoek verklaart waarom het eten van uitwerpselen van vitaal belang kan zijn voor de overleving van vogels
- Hoe algen geheugen gebruiken om zich te beschermen tegen plotselinge veranderingen in zonlicht
- Wat is een reden waarom de classificatie van protisten in één koninkrijk moeilijk is?
- Muizen helpen onderzoekers onderzoeken hoe het dieet van koeien het melkvetgehalte beïnvloedt
- Voorbeelden van sensorische aanpassing
- Origami inspireert nieuwe technologie voor weefselregeneratie

- Katalysatoronderzoek voor zonnebrandstoffen:amorf molybdeensulfide werkt het beste

- Nieuw elektronisch apparaat detecteert explosieve dampen

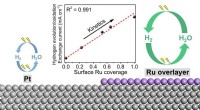
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
- Bonddissociatie-energieën voor overgangsmetaalsiliciden nauwkeurig bepaald

 Hoe u energiezuinig licht kunt upcyclen:een nieuw ontwerp voor zeer efficiënte conversiematerialen
Hoe u energiezuinig licht kunt upcyclen:een nieuw ontwerp voor zeer efficiënte conversiematerialen  Hoe het plasmamembraan regelt wat er in komt en uit een cel komt
Hoe het plasmamembraan regelt wat er in komt en uit een cel komt  Onderzoek onderzoekt waarom mensen eerder van etniciteit veranderen
Onderzoek onderzoekt waarom mensen eerder van etniciteit veranderen  Waarom is het belangrijk om beweging te bestuderen?
Waarom is het belangrijk om beweging te bestuderen?  Een verhaal over het overleven van zaden:hoe bomen 'vrienden' dichtbij houden en 'vijanden' gissen
Een verhaal over het overleven van zaden:hoe bomen 'vrienden' dichtbij houden en 'vijanden' gissen  Onderzoekers ontwikkelen een mechanisme voor elektrische 180 ° -schakeling van de Néel-vector in een spin-splitsende antiferromagneet
Onderzoekers ontwikkelen een mechanisme voor elektrische 180 ° -schakeling van de Néel-vector in een spin-splitsende antiferromagneet  Slimme technologie kan de sleutel zijn tot veiligere winterwegen
Slimme technologie kan de sleutel zijn tot veiligere winterwegen Waarom is warm water minder dicht dan koud water?
Waarom is warm water minder dicht dan koud water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

