
Wetenschap
Welke moleculaire verbinding ioniseert in water?
1. Zoutzuur (HCl)
- Wanneer HCl oplost in water, valt het volledig uiteen in waterstofionen (H+) en chloride-ionen (Cl-).
2. Natriumhydroxide (NaOH)
- NaOH dissocieert in water en vormt natriumionen (Na+) en hydroxide-ionen (OH-).
3. Zwavelzuur (H2SO4)
- H2SO4 is een sterk zuur dat zich splitst in twee waterstofionen (2H+) en één sulfaation (SO42-).
4. Azijnzuur (CH3COOH)
- Azijnzuur ondergaat een gedeeltelijke dissociatie in water, waarbij waterstofionen (H+) en acetaationen (CH3COO-) worden gevormd.
5. Ammoniumhydroxide (NH4OH)
- NH4OH valt uiteen in ammoniumionen (NH4+) en hydroxide-ionen (OH-).
Dit zijn slechts enkele voorbeelden van veel moleculaire verbindingen die ionisatie in water ondergaan. Het vermogen van een moleculaire verbinding om in water te ioniseren hangt af van de chemische structuur en de polariteit van het watermolecuul.
 Publiek verward door berichten over klimaatverandering
Publiek verward door berichten over klimaatverandering Kan housemuziek de energiecrisis oplossen?
Kan housemuziek de energiecrisis oplossen? Iraakse Koerdische boeren vechten tegen droogte terwijl Lake Dukan zich terugtrekt
Iraakse Koerdische boeren vechten tegen droogte terwijl Lake Dukan zich terugtrekt Duitsland zou over 10 jaar de laatste gletsjers kunnen verliezen
Duitsland zou over 10 jaar de laatste gletsjers kunnen verliezen Hoe het aanpakken van invasieve soorten op het land tot 'verbluffende' verbeteringen op zee kan leiden
Hoe het aanpakken van invasieve soorten op het land tot 'verbluffende' verbeteringen op zee kan leiden
Hoofdlijnen
- Hoe gisten erin slagen de genetische onbalans van extra chromosomen te compenseren
- Nieuw onderzoek heeft uitgewezen dat virussen ogen en oren op ons kunnen richten
- Voorspellen wat uitsterven kan betekenen voor lemuren en de bossen die ze thuis noemen
- Inheemse voedselsoevereiniteit vereist betere en nauwkeurigere gegevensverzameling
- Hoe klimaatverandering planten onder druk zet en hun groei verandert
- Scheepsreus verandert koers om walvissen in Sri Lanka te redden
- Bedreiging van de opwarming van de aarde voor koraalriffen:kunnen sommige soorten zich aanpassen?
- Sociale vleermuizen betalen een prijs:schimmelziekte, witte-neussyndroom... uitsterven?
- Windparken langs bergruggen kunnen vleermuizen negatief beïnvloeden
- Een fluorogene sonde kan de activiteit van multiresistente pathogenen in een testsysteem detecteren
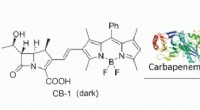
- Nieuwe chemische modificatie van een natuurlijke verbinding voor de behandeling van kanker

- Nieuw zonnemateriaal kan drinkwater reinigen

- Nieuwe moleculaire sondes voor opioïde receptoren

- Ladingsdragers volgen in het moleculaire kristal op organische pn-junctie
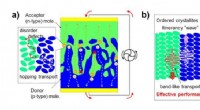
 Een snelheidsrecord van 130 km/uur voor gletsjerbreuk helpt de fysica van het instorten van de ijskap te onthullen
Een snelheidsrecord van 130 km/uur voor gletsjerbreuk helpt de fysica van het instorten van de ijskap te onthullen  Asteroïdenregen op het aarde-maansysteem 800 miljoen jaar geleden onthuld door maankraters
Asteroïdenregen op het aarde-maansysteem 800 miljoen jaar geleden onthuld door maankraters Vier kenmerken van Carbon
Vier kenmerken van Carbon Wat is de oorzaak en het resultaat van rotatiebeweging?
Wat is de oorzaak en het resultaat van rotatiebeweging?  Italië neemt Alitalia over als reactie op virus
Italië neemt Alitalia over als reactie op virus Hoe valentie van elektronen in het periodiek systeem te berekenen
Hoe valentie van elektronen in het periodiek systeem te berekenen  Pitch-definitie (fysica): frequentie van geluid begrijpen
Pitch-definitie (fysica): frequentie van geluid begrijpen  Met welke uitdagingen worden geologen geconfronteerd?
Met welke uitdagingen worden geologen geconfronteerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

