
Wetenschap
Wat is de massa van 0,92 mol aluminiumchromaat?
De atoommassa van aluminium (Al) is 26,98 g/mol.
De atoommassa van chroom (Cr) is 51,996 g/mol.
De atoommassa van zuurstof (O) is 15,999 g/mol.
In aluminiumchromaat zijn er 2 atomen aluminium, 3 atomen chroom en 12 zuurstofatomen. De molaire massa van aluminiumchromaat kan dus als volgt worden berekend:
Molaire massa van Al2(CrO4)3 =2(26,98 g/mol) + 3(51,996 g/mol) + 12(15,999 g/mol)
=54,96 g/mol + 155,988 g/mol + 191,988 g/mol
=402,936 g/mol
Nu kunnen we de massa van 0,92 mol aluminiumchromaat berekenen door de molaire massa ervan te vermenigvuldigen met het aantal mol:
Massa =0,92 mol * 402,936 g/mol
=371,344 gram
Daarom is de massa van 0,92 mol aluminiumchromaat ongeveer 371,344 g.
Hoofdlijnen
- Inzicht in de ademhaling van planten:onderzoek identificeert de belangrijkste eiwitinteractie achter ritmische stomatale bewegingen
- Wat gebeurt er als de celcyclus niet langer gereguleerd wordt?
- Vooruitgang in de genomica van populieren:vrijwel naadloze genoomassemblage onthult nieuwe inzichten en toepassingen
- Verschillen tussen codering en sjabloonstrengen
- Wanneer een organisme zoals gist leeft door fermentatie, zet het pyrodruivenzuur uit glycolsis om in een andere samengestelde alcohol. Waarom direct uitscheiden?
- Uw smartphone is mogelijk gelinkt aan krokodillenaanvallen in Indonesië
- Nieuw onderzoek laat zien wat vissen onder het ijs van plan zijn
- Wat zijn de interne organen van het skeletstelsel?
- Wat is een chromosoom?
- Batterijen verborgen laag onthuld
- Onderzoekers laten zien hoe mengsels van biomoleculen communiceren, interageren en zich aanpassen aan hun omgeving

- Nieuwe eiwitstudie verbreedt kennis van moleculaire basis voor ziekte

- Een eiwit dat zichzelf repliceert

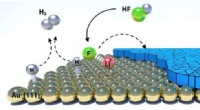
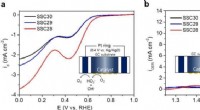
- Onderzoekers ontwikkelen hoogwaardige perovskietoxide-katalysatoren met behulp van laat-overgangsmetaaloxidematerialen
 LHCb ontdekt drie nieuwe exotische deeltjes:de pentaquark en het allereerste paar tetraquarks
LHCb ontdekt drie nieuwe exotische deeltjes:de pentaquark en het allereerste paar tetraquarks Insight-HXMT geeft inzicht in de oorsprong van snelle radioflitsen
Insight-HXMT geeft inzicht in de oorsprong van snelle radioflitsen Vriend of vijand? Civiele drones zorgen voor discussie
Vriend of vijand? Civiele drones zorgen voor discussie  Draag OS-smartwatches om nieuwe Qualcomm-chipboosts te krijgen
Draag OS-smartwatches om nieuwe Qualcomm-chipboosts te krijgen Luisteraars kunnen zich aanpassen aan sprekerspecifieke akoestiek, studieprogramma's
Luisteraars kunnen zich aanpassen aan sprekerspecifieke akoestiek, studieprogramma's  De greep van India op steenkool losmaken zonder de miljoenen in de steek te laten die erop vertrouwen
De greep van India op steenkool losmaken zonder de miljoenen in de steek te laten die erop vertrouwen VS worden geconfronteerd met een groter wordende informatiekloof over nanotechnologie
VS worden geconfronteerd met een groter wordende informatiekloof over nanotechnologie Dreiging van bovenaf:race door om de verdediging van drones te versterken
Dreiging van bovenaf:race door om de verdediging van drones te versterken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


