
Wetenschap
Hoeveel zilverfosfaat wordt geproduceerd als 10 g acetaat reageert met een teveel aan natriumfosfaat?
2AgCH3COO(aq) + Na3PO4(aq) → Ag3PO4(s) + 3CH3COONa(aq)
Uit de vergelijking kunnen we zien dat 2 mol zilveracetaat reageert met 1 mol natriumfosfaat. De molaire massa van zilveracetaat is 166,91 g/mol en de molaire massa van natriumfosfaat is 163,94 g/mol. Daarom is 10 g zilveracetaat:
10 g / 166,91 g/mol =0,0599 mol
Omdat we een teveel aan natriumfosfaat hebben, kunnen we aannemen dat al het zilveracetaat zal reageren. Volgens de uitgebalanceerde vergelijking zal 0,0599 mol zilveracetaat 0,0299 mol zilverfosfaat produceren. De molmassa van zilverfosfaat is 418,67 g/mol, dus de geproduceerde massa zilverfosfaat is:
0,0299 mol * 418,67 g/mol =12,54 g
Als 10 g zilveracetaat reageert met een overmaat natriumfosfaat, wordt er dus 12,54 g zilverfosfaat geproduceerd.
 Wat de houding van vogels ten opzichte van zwerfvuil ons vertelt over hun aanpassingsvermogen
Wat de houding van vogels ten opzichte van zwerfvuil ons vertelt over hun aanpassingsvermogen  Droogte verstevigt de greep op Marokko
Droogte verstevigt de greep op Marokko VN:toezeggingen CO2-reductie door landen lang niet genoeg
VN:toezeggingen CO2-reductie door landen lang niet genoeg Kleiner dan verwacht fytoplankton kan betekenen dat er minder koolstof wordt vastgelegd op de zeebodem
Kleiner dan verwacht fytoplankton kan betekenen dat er minder koolstof wordt vastgelegd op de zeebodem Veranderingen in landbedekking hebben de droogte in de Dust Bowl waarschijnlijk geïntensiveerd
Veranderingen in landbedekking hebben de droogte in de Dust Bowl waarschijnlijk geïntensiveerd
Hoofdlijnen
- Disruptieve bio-engineering - verandert de manier waarop cellen met elkaar omgaan
- Onderzoekers voeren een nieuwe analyse van het tarwemicrobioom uit onder vier managementstrategieën
- Honden hoe oorlog werkt
- Luie valsspeler leeft onder de grond,
- Nieuw inzicht in het selecteren van geschikte primers en databases bij het sequencen van bodemaaltjes-DNA
- Hoe transcriptie epigenetische silencing oplevert
- Soorten forensische tests
- Indringende vraag:Waarom worden albino's altijd als schurken neergezet?
- Prokaryotische cellen: definitie, structuur, functie (met voorbeelden)
- Forensische wetenschappers herstellen menselijk DNA van muggen

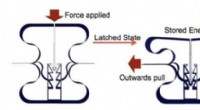
- Wetenschappers ontwerpen materiaal dat energie kan opslaan als een adelaarsgreep
- Nieuwe theorie ontsluit het geheim achter eiwit-membraan-interacties

- Beoordeling van het begin van calciumfosfaatkiemvorming door gehyperpolariseerde real-time NMR

- Engineering van een nieuwe draai voor ziektediagnostiek

 Nieuwe gegevens over onderwatervulkanen in Bransfield Strait, Antarctica
Nieuwe gegevens over onderwatervulkanen in Bransfield Strait, Antarctica Wat levert meer energie op:één kilogram steenkool of uranium?
Wat levert meer energie op:één kilogram steenkool of uranium?  Nieuwe benadering voor het vangen van van tumor afgeleide exosomen uit een prostaatkankercellijn
Nieuwe benadering voor het vangen van van tumor afgeleide exosomen uit een prostaatkankercellijn Waar zijn alle koolstofatomen in een ring van glucose?
Waar zijn alle koolstofatomen in een ring van glucose?  Structuur van het spierenstelsel
Structuur van het spierenstelsel Negen doden nadat Indonesische hoofdstad getroffen werd door nieuwjaarsoverstroming (Update)
Negen doden nadat Indonesische hoofdstad getroffen werd door nieuwjaarsoverstroming (Update) Binnenkort in huis:3D-voedselprinters, nano-voedsel en insectenburgers
Binnenkort in huis:3D-voedselprinters, nano-voedsel en insectenburgers Cassini-missie onthulde de geheimen van Saturnus
Cassini-missie onthulde de geheimen van Saturnus
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

