
Wetenschap
Wat is het elektronendomein van CH2O?
Om het elektronendomein van CH2O te bepalen, moeten we rekening houden met het aantal elektronenparen rond het centrale atoom, koolstof (C). In CH2O is koolstof gebonden aan twee waterstofatomen (H) en één zuurstofatoom (O). Elke enkele binding tussen koolstof en waterstof vertegenwoordigt één elektronenpaar, en de dubbele binding tussen koolstof en zuurstof vertegenwoordigt twee elektronenparen. Daarom heeft koolstof vier elektronenparen eromheen.
Wanneer er vier elektronenparen rond een centraal atoom zijn, is het elektronendomein tetraëdrisch. Dit betekent dat de vier elektronenparen zichzelf in een tetraëdrische vorm rangschikken, met het centrale atoom in het midden en de elektronenparen gericht naar de hoeken van een tetraëder.
 Duurzaamheid en efficiëntie:de nieuwe trends in de kunststofindustrie
Duurzaamheid en efficiëntie:de nieuwe trends in de kunststofindustrie Is de pH van 13 een zwak zuur of een sterke base?
Is de pH van 13 een zwak zuur of een sterke base?  Onderzoekers gebruiken zijde van zijderupsen om spierweefsel te modelleren
Onderzoekers gebruiken zijde van zijderupsen om spierweefsel te modelleren Is bariumchloride oplosbaar in water?
Is bariumchloride oplosbaar in water?  Welke conversiefactor voor natrium wordt gebruikt om de massa-mol te veranderen?
Welke conversiefactor voor natrium wordt gebruikt om de massa-mol te veranderen?
 Zijn onze botten goed ontworpen? Insecten en krabben hebben een voorsprong op ons
Zijn onze botten goed ontworpen? Insecten en krabben hebben een voorsprong op ons  Overmatig gebruik van water bedreigt wereldwijde voedselvoorziening
Overmatig gebruik van water bedreigt wereldwijde voedselvoorziening Onderzoekers rangschikken landen op uitstoot van olieproductie
Onderzoekers rangschikken landen op uitstoot van olieproductie Hoe kleur bepaalt welke dieren we vrezen – en beschermen
Hoe kleur bepaalt welke dieren we vrezen – en beschermen  Ongekende aard van extreme overstromingen in Noordwest-Engeland onthuld
Ongekende aard van extreme overstromingen in Noordwest-Engeland onthuld
Hoofdlijnen
- Matchmaking met gevolgen
- Hoe zijn de vorm en afmetingen van laboratoriumapparatuur met bekerglas gerelateerd aan hun functie?
- Wetenschappers vinden bewijs van onze beste vrienden, honden, op dezelfde manier aangepast aan malaria in Afrika
- Welke oplossingen vind je in het menselijk lichaam?
- Het opzetten van een genoombrede kaart van bacteriële genen die cruciaal zijn voor de kolonisatie van planten door nuttige microben
- Tropische en woestijngrassen kunnen verder naar het zuiden migreren
- Hoe zijn eencellige organismen beter dan meercellige organismen?
- Wat maakt pinguïnveren ijsbestendig?
- Een reisbrochure van Science Cell maken
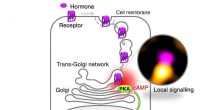
- Hoe receptoren voor medicijnen in cellen werken
- Nieuw glow-in-the-dark materiaal kan pad van drugs door het menselijk lichaam volgen

- Keramische honingraatluchtfilters kunnen stadsvervuiling verminderen

- Een weg om defecten tijdens additive manufacturing te vermijden

- UNESCO viert 150 jaar scheikunde periodiek systeem

 Video:Eclipse-ballonvaartproject
Video:Eclipse-ballonvaartproject Hard kauwen:waarom kauwen een cruciale rol speelde in de evolutie
Hard kauwen:waarom kauwen een cruciale rol speelde in de evolutie  Hoe je statische elektriciteit opbouwt met je handen
Hoe je statische elektriciteit opbouwt met je handen Wat is er met onze beloofde vrije tijd gebeurd? En vinden we die in de slimme stad?
Wat is er met onze beloofde vrije tijd gebeurd? En vinden we die in de slimme stad? De noordelijke permafrostregio stoot meer broeikasgassen uit dan het opvangt, zo blijkt uit onderzoek
De noordelijke permafrostregio stoot meer broeikasgassen uit dan het opvangt, zo blijkt uit onderzoek  Nieuwe soliton-laserpulsen leveren hoge energie in een biljoenste van een seconde
Nieuwe soliton-laserpulsen leveren hoge energie in een biljoenste van een seconde Accelerator op een chip gedemonstreerd
Accelerator op een chip gedemonstreerd De voor- en nadelen van supergeleiders
De voor- en nadelen van supergeleiders
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

