
Wetenschap
Wanneer een stof bevriest, wat zorgt er dan voor dat de vloeibare fase overgaat in de vaste fase?
Naarmate de temperatuur van een vloeistof wordt verlaagd, vertragen de moleculen en raken ze dichter op elkaar gepakt. De aantrekkingskrachten tussen de moleculen, zoals waterstofbruggen, van der Waals-krachten en ionische bindingen, worden sterker en beginnen de kinetische energie van de moleculen, wat de energie van hun beweging is, te overwinnen.
Wanneer de aantrekkingskrachten sterk genoeg worden om de kinetische energie te overwinnen, kunnen de moleculen niet langer vrij bewegen en raken ze opgesloten in een vaste positie. Hierdoor verandert de vloeistof in een vaste stof. De vaste fase heeft een bepaalde vorm en volume, en de moleculen zijn in een regelmatig patroon gerangschikt.
Het vriespunt van een vloeistof is de temperatuur waarbij de vloeibare en vaste fasen in evenwicht zijn. Bij deze temperatuur is de bevriezingssnelheid gelijk aan de smeltsnelheid en is er geen netto verandering in de hoeveelheid vaste en vloeibare fasen.
 Oceaancirculatie is de sleutel tot het begrijpen van onzekerheden in voorspellingen van klimaatverandering
Oceaancirculatie is de sleutel tot het begrijpen van onzekerheden in voorspellingen van klimaatverandering Dammen of niet dammen? Pakistan-experts denken na over de overstromingsstrategie
Dammen of niet dammen? Pakistan-experts denken na over de overstromingsstrategie  De mensheid moet oceanen redden om zichzelf te redden, VN waarschuwt
De mensheid moet oceanen redden om zichzelf te redden, VN waarschuwt Royalty's voor wilde dieren:een toekomst voor natuurbehoud?
Royalty's voor wilde dieren:een toekomst voor natuurbehoud?  Onderzoek voorspelt dat extreme branden steeds meer deel zullen uitmaken van ons wereldwijde landschap
Onderzoek voorspelt dat extreme branden steeds meer deel zullen uitmaken van ons wereldwijde landschap
Hoofdlijnen
- Stille mutaties helpen bacteriën antibiotica te ontwijken
- Hoe een interne lichaamsklok spoelwormen vrijhoudt van constipatie
- Hoe bacteriën hun onzichtbaarheidsmantels hechten aan het immuunsysteem
- Een verklaring van het skeletsysteem
- Grootte is belangrijk:hoe lichaamsgrootte de verouderingspatronen van honden bepaalt
- Hoe markergenen in celclusters te vinden
- 'Junk'-wetenschap? Voor sommige krabben doet de grootte er in ieder geval toe
- Multiresistentie tegen antibiotica:waarom bacteriën zo effectief zijn
- Waarom gaan leerlingen met een handicap naar 'speciale scholen' als onderzoek ons leert dat ze beter kunnen presteren in het reguliere systeem?
- Biocompatibele fotonische kristallen breiden toepassingen uit van optica tot medicijnen
- Video:U gebruikt desinfectiemiddelen verkeerd. Dit is wat je echt moet doen

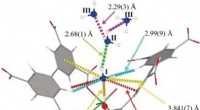
- Een robuust materiaal voor de opname en opslag van ammoniak met dichtheden die dicht bij die van het vloeibaar gemaakte gas liggen
- Hoog rijden? Chemici zetten stappen richting marihuana-ademanalysator

- Nieuw katalysatormateriaal produceert overvloedige goedkope waterstof

 Natuurkundigen onthullen waarom materie het universum domineert
Natuurkundigen onthullen waarom materie het universum domineert  Is straf wel zo effectief als we denken?
Is straf wel zo effectief als we denken? Waarom dromen we?
Waarom dromen we?  Een oude mastodont ontstak een debat over de aankomst van mensen in Noord-Amerika
Een oude mastodont ontstak een debat over de aankomst van mensen in Noord-Amerika De druk staat nu op Facebook om politieke advertenties te verbieden, te
De druk staat nu op Facebook om politieke advertenties te verbieden, te De typen zeebodembodems
De typen zeebodembodems  Fitness-app onthulde gegevens over militaire, inlichtingenpersoneel
Fitness-app onthulde gegevens over militaire, inlichtingenpersoneel Oceanografische analyse biedt potentiële crashlocatie van MH370
Oceanografische analyse biedt potentiële crashlocatie van MH370
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

