
Wetenschap
Wat zou het verschil zijn tussen vaste stoffen die worden verkregen door het verdampen van een oplossing van vaste stof tot droogheid en het laten afkoelen totdat het kristalliseert?
Verdamping tot droogheid:
- Wanneer een oplossing van een vaste stof tot droog wordt verdampt, wordt het oplosmiddel (meestal water) volledig verwijderd, waardoor de vaste opgeloste stof in een sterk geconcentreerde vorm achterblijft. Het snelle verdampingsproces laat niet voldoende tijd toe voor de vorming van grote, goed gedefinieerde kristallen.
- De resulterende vaste stof is doorgaans een fijn poeder of amorfe massa, bestaande uit zeer kleine, onregelmatig gevormde kristallen of zelfs individuele moleculen. Het ontbreken van een kristalstructuur maakt het gevoeliger voor aankoeken en klonteren.
- De afwezigheid van oplosmiddel betekent dat de vaste stof verkregen door verdamping tot droogte een hogere concentratie van de opgeloste stof heeft vergeleken met kristallen gevormd door kristallisatie.
Kristalisatie door koeling:
- In het geval van kristallisatie door afkoeling wordt de oplossing langzaam afgekoeld, waardoor de opgeloste moleculen geleidelijk uit de oplossing kunnen komen en zichzelf kunnen rangschikken in een regelmatige, geordende structuur, bekend als een kristalrooster.
- Naarmate de temperatuur daalt, neemt de oplosbaarheid van de opgeloste stof af, waardoor deze uit de oplossing neerslaat in de vorm van goed gedefinieerde, grotere kristallen.
- De door afkoeling gevormde kristallen zijn doorgaans groter van formaat en hebben een meer regelmatige vorm, met facetten en gedefinieerde kristalvlakken. Ze zijn minder gevoelig voor aankoeken en klonteren vanwege hun georganiseerde structuur.
- De aanwezigheid van resterend oplosmiddel in de door koeling verkregen kristallen kan hun samenstelling en eigenschappen beïnvloeden.
Overzichtstabel:
| Kenmerkend | Verdamping tot droogheid | Kristallisatie door koeling |
|---|---|---|
| Kristalgrootte en structuur | Kleine, onregelmatige kristallen of amorfe massa | Grotere, goed gedefinieerde kristallen met regelmatige vorm |
| Neiging tot klonteren en klonteren | Grotere kans op aankoeken en klonteren | Minder kans op aankoeken en klonteren |
| Concentratie van opgeloste stof | Hogere concentratie door volledige verwijdering van oplosmiddel | Lagere concentratie door resterend oplosmiddel |
| Uiterlijk | Fijn poeder of amorf materiaal | Grotere, individuele kristallen met verschillende vormen |
Concluderend kunnen we stellen dat de vaste stoffen die worden verkregen door een oplossing droog te laten verdampen en deze te laten kristalliseren door afkoeling hoofdzakelijk verschillen in hun kristalgrootte, structuur en neiging tot klonteren. De gewenste eigenschappen en het beoogde gebruik van de vaste stof bepalen welke methode geschikter is.
 Kijken naar een medicijn in actie:precieze werking antikankermedicijnen in de cel opgehelderd
Kijken naar een medicijn in actie:precieze werking antikankermedicijnen in de cel opgehelderd Wanneer suiker kan worden opgelost in één kopje water?
Wanneer suiker kan worden opgelost in één kopje water?  Test voor Benzeen
Test voor Benzeen  Rekbare en knijpende zachte sensoren een stap dichterbij dankzij nieuwe hechtmethode
Rekbare en knijpende zachte sensoren een stap dichterbij dankzij nieuwe hechtmethode Wat is het formule-ion dat wordt gevormd wanneer calcium een edelgas-elektronenconfiguratie bereikt?
Wat is het formule-ion dat wordt gevormd wanneer calcium een edelgas-elektronenconfiguratie bereikt?
 Het werk van God, of dat van de mens? De door storm geteisterde Louisianen zijn onzeker
Het werk van God, of dat van de mens? De door storm geteisterde Louisianen zijn onzeker  Brandweerlieden in Australië racen om branden te bedwingen terwijl hittegolf opdoemt
Brandweerlieden in Australië racen om branden te bedwingen terwijl hittegolf opdoemt Nieuw onderzoek suggereert dat wereldwijde herbebossingsinspanningen een langetermijnvisie moeten hebben
Nieuw onderzoek suggereert dat wereldwijde herbebossingsinspanningen een langetermijnvisie moeten hebben Brexit kan Wales transformeren van schapenboerderijen naar bos
Brexit kan Wales transformeren van schapenboerderijen naar bos Lijkschouwers kunnen het niet eens worden over de oorzaak van iemands dood
Lijkschouwers kunnen het niet eens worden over de oorzaak van iemands dood
Hoofdlijnen
- Processen die ATP
- Waarom is het zo moeilijk voor soorten om hun ecologische niche te verlaten?
- Hoe menselijke cellen en pathogene shigella de strijd aangaan
- Second Life-gegevens bieden inzicht in hoe trends zich verspreiden
- Welke term beschrijft een proces dat alleen plaatsvindt in meercellige organismen en waarbij cellen verschillende gespecialiseerde functies hebben?
- Worden aminozuren slechts door één codon weergegeven?
- Helder en fotostabiel groen fluorescerend eiwit afgeleid van Japanse kwallen
- Hebben hersencellen een lipide-dubbellaag?
- Hoe krijgen mensen stikstof in hun lichaam?
- Blootstelling aan pesticiden meetbaar via rioolwater

- Exoskeletale microstructuur van extreem harde kokoskrabklauwen

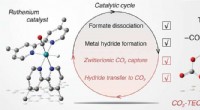
- Monitoring van tussenproducten in CO2-conversie naar formiaat door metaalkatalysator
- De natuur biedt een sleutel tot het afstoten van vloeistoffen

- Onderzoekers gebruiken kunstmatige neurale netwerken om het testen van materialen te stroomlijnen

 Hoe bittere koude winteruitbarstingen en een opwarmende planeet de kustlijn van Lake Michigan zullen opvreten?
Hoe bittere koude winteruitbarstingen en een opwarmende planeet de kustlijn van Lake Michigan zullen opvreten? Boeren in Australië verwelkomen hulp bij regen tijdens ernstige droogte
Boeren in Australië verwelkomen hulp bij regen tijdens ernstige droogte Waarom boetes en gevangenisstraffen het gedrag van de minibuschauffeurs in Ghana niet zullen veranderen?
Waarom boetes en gevangenisstraffen het gedrag van de minibuschauffeurs in Ghana niet zullen veranderen? Welke vorm van bacterie is tyfus?
Welke vorm van bacterie is tyfus?  Parken helpen steden – maar alleen als mensen ze gebruiken
Parken helpen steden – maar alleen als mensen ze gebruiken Onderzoeker:Waarom is Australië, nu er een wrede zomer in het verschiet ligt, zo onvoorbereid?
Onderzoeker:Waarom is Australië, nu er een wrede zomer in het verschiet ligt, zo onvoorbereid?  Idaho, Energieministerie tekent deal over verbruikte splijtstof
Idaho, Energieministerie tekent deal over verbruikte splijtstof Trump terugdraaien van kilometerstandnormen lef klimaatverandering push (update)
Trump terugdraaien van kilometerstandnormen lef klimaatverandering push (update)
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

