
Wetenschap
Ontleding van een metaalcarbonaat bij verhitting?
Metaalcarbonaat (MCO3) → Metaaloxide (MO) + Kooldioxide (CO2)
Hier vertegenwoordigt M het metaal dat aanwezig is in de carbonaatverbinding.
Wanneer calciumcarbonaat (CaCO3), algemeen bekend als kalksteen of krijt, bijvoorbeeld wordt verwarmd, valt het uiteen in calciumoxide (CaO) en kooldioxidegas:
CaCO3 (calciumcarbonaat) → CaO (calciumoxide) + CO2 (kooldioxide)
Terwijl het calciumcarbonaat wordt verwarmd, wordt de carbonaatgroep (CO32-) afgebroken, waardoor kooldioxidegasmoleculen vrijkomen. De resterende calciumionen (Ca2+) combineren met zuurstofionen (O2-) om calciumoxide te vormen, een stabiele metaaloxideverbinding.
Deze ontledingsreactie is belangrijk bij verschillende industriële processen, zoals de productie van ongebluste kalk (calciumoxide) voor bouwmaterialen, de reductie van metaalertsen om metalen te verkrijgen en de productie van cement en glas. Het begrijpen van het ontledingsgedrag van metaalcarbonaten is ook essentieel op gebieden als geologie, metallurgie en materiaalkunde.
 Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren
Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren PH niveau van regenwater
PH niveau van regenwater
Regenwater is van nature enigszins zuur, met een pH van ongeveer 5,0. Natuurlijke variaties en menselijke vervuilers kunnen ervoor zorgen dat de regen zuurder wordt. Afhankelijk van de regio, het seizoen en de aanwezigheid
 UNESCO viert 150 jaar scheikunde periodiek systeem
UNESCO viert 150 jaar scheikunde periodiek systeem 3 Waarom is het belangrijk dat er tijdens de destillatie een stroom koel water rond de condensor stroomt?
3 Waarom is het belangrijk dat er tijdens de destillatie een stroom koel water rond de condensor stroomt?  Kunstkraakbeen onder spanning zo sterk als natuurlijk materiaal
Kunstkraakbeen onder spanning zo sterk als natuurlijk materiaal
 Brekende golven en vochttransport zorgen voor extreme neerslag
Brekende golven en vochttransport zorgen voor extreme neerslag Nieuw rapport onderzoekt de veiligheid van het gebruik van dispergeermiddelen bij het opruimen van olievlekken
Nieuw rapport onderzoekt de veiligheid van het gebruik van dispergeermiddelen bij het opruimen van olievlekken Vulkanisch gordijn van vuur jaagt mensen op de vlucht voor huizen in Hawaï
Vulkanisch gordijn van vuur jaagt mensen op de vlucht voor huizen in Hawaï De bijdrage van de luchtvaart aan het terugdringen van de klimaatverandering zal waarschijnlijk klein zijn
De bijdrage van de luchtvaart aan het terugdringen van de klimaatverandering zal waarschijnlijk klein zijn Eerste twee op natuur gebaseerde waterretentiemaatregelen zijn operationeel in Hongarije
Eerste twee op natuur gebaseerde waterretentiemaatregelen zijn operationeel in Hongarije
Hoofdlijnen
- Hoe moleculaire riboswitches werken in bacteriën
- Hoe pittig wordt mosterd afhankelijk van de grondsoort?
- Discovery onthult hoe planten cellulose maken voor kracht en groei
- Nieuw onderzoek wijst uit waarom sommige microbiële genen meer promiscue zijn dan andere
- Staan we aan het begin van het einde van de westerse beschaving?
- Meld-en-klauwzeer:de lacunes in de inspanningen van Zuid-Afrika om het onder controle te houden
- Hoe verhoudt het scheppingsverhaal zich tot de celtheorie?
- Honingbijen stemmen om te beslissen over nestplaatsen – waarom we zouden moeten luisteren
- Welke mRNA-codons zullen het translatieproces starten?
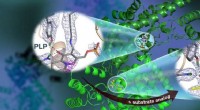
- Neutronen observeren vitamine B6-afhankelijke enzymactiviteit die nuttig is voor de ontwikkeling van geneesmiddelen
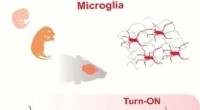
- Microglia in hersenweefsel visualiseren met een fluorescentie-aanzetsubstraat
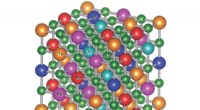
- Ongeordende materialen kunnen het moeilijkst zijn, meest hittebestendige carbiden
- Schimmelinfectie van het hoornvlies behandelen met synthetische moleculen

- Upcycling van sponsachtig plastic schuim van schoenen, matrassen en isolatie

 Als de reactanten van een reactie één S- en vier O-atomen hebben, wat zal het product dan hebben?
Als de reactanten van een reactie één S- en vier O-atomen hebben, wat zal het product dan hebben?  Onderzoeksteam zet het vuur op 3D-printinkten
Onderzoeksteam zet het vuur op 3D-printinkten Studie:Hoe prijzen en middelen voor cloud computing te berekenen
Studie:Hoe prijzen en middelen voor cloud computing te berekenen  Als auto 1 een grotere traagheid heeft dan auto 2, dan heeft dat?
Als auto 1 een grotere traagheid heeft dan auto 2, dan heeft dat?  Personalisatie van online diensten:Nuttig maatwerk of heimelijke manipulatie?
Personalisatie van online diensten:Nuttig maatwerk of heimelijke manipulatie? Platina nanodeeltjes voor selectieve behandeling van leverkankercellen
Platina nanodeeltjes voor selectieve behandeling van leverkankercellen Wat is het verschil tussen een bijtschildpad en een geschilderde schildpad?
Wat is het verschil tussen een bijtschildpad en een geschilderde schildpad?  Witte Huis krijgt rapport dat automatische tarieven zou kunnen activeren
Witte Huis krijgt rapport dat automatische tarieven zou kunnen activeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

