
Wetenschap
Wat maakt een samengestelde base?
De sterkte van een base wordt bepaald door zijn vermogen om hydroxide-ionen te doneren. Hoe meer hydroxide-ionen een base kan doneren, hoe sterker deze is. Enkele veel voorkomende samengestelde basen zijn onder meer:
* Natriumhydroxide (NaOH)
* Kaliumhydroxide (KOH)
* Calciumhydroxide (Ca(OH)2)
* Ammoniumhydroxide (NH4OH)
Deze basen zijn allemaal sterke basen, wat betekent dat ze volledig dissociëren in water, waarbij hydroxide-ionen vrijkomen.
Zwakke basen dissociëren daarentegen slechts gedeeltelijk in water. Enkele veel voorkomende zwakke basen zijn onder meer:
* Ammoniak (NH3)
* Koolzuur (H2CO3)
* Azijnzuur (CH3COOH)
Wanneer deze basen in water worden opgelost, komen er slechts gedeeltelijk hydroxide-ionen vrij. Dit betekent dat hun pH lager is dan die van sterke basen.
De concentratie hydroxide-ionen in een oplossing wordt gemeten met de pH-schaal. De pH-schaal varieert van 0 tot 14, waarbij een pH van 7 neutraal is. Een pH lager dan 7 duidt op een zure oplossing, terwijl een pH hoger dan 7 duidt op een basische oplossing.
Samengestelde basen zijn belangrijk in een verscheidenheid aan toepassingen, waaronder:
* Reinigingsproducten:Samengestelde basen worden vaak gebruikt in schoonmaakproducten omdat ze vuil en roet kunnen afbreken.
* Deodorants:Samengestelde basen kunnen in deodorants worden gebruikt om de door zweet geproduceerde zuren te neutraliseren.
* Farmaceutische producten:Samengestelde basen worden gebruikt in een verscheidenheid aan farmaceutische producten, waaronder maagzuurremmers en laxeermiddelen.
Samengestelde basen zijn essentieel voor veel industrieën en worden in een grote verscheidenheid aan toepassingen gebruikt.
Hoofdlijnen
- Paring induceert seksuele remming bij vrouwelijke springspinnen
- Puin van de tsunami van 2011 bracht honderden soorten over de Stille Oceaan
- Welke soorten cellen zijn bacteriën?
- Mycoheterotrofe planten als sleutel tot het Wood Wide Web
- Oud skelet-DNA suggereert genetische link met eerste mensen in Noord-Amerika
- Moleculaire kaart laat zien hoe gevaarlijke biowapens kunnen worden uitgeschakeld
- Stelt de celtheorie dat alle cellen voortkomen uit andere cellen?
- Onderzoekers onthullen de dynamische structuur van FLVCR-eiwitten en hun functie bij het transport van voedingsstoffen
- Grootte doet er niet toe - althans voor hamerhaaien en zwemprestaties
- Nieuw celmembraanmodel kan de sleutel zijn tot het ontdekken van nieuwe eiwiteigenschappen
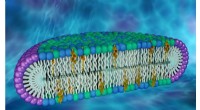
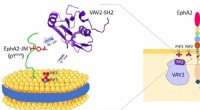
- Wetenschappers onthullen dubbele specificiteit van Vav2-SH2-eiwit
- Meteorietinslagen kunnen een onverwachte vorm van silica veroorzaken
- Onthulling van de nare werking van transvetzuren in het bloed

- Nieuwe recensie benadrukt innovatieve katalysatoren:ontwerp en toepassing
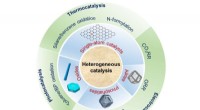
 Helling van een geplotte lijn vinden met de TI-84 Plus Silver Edition
Helling van een geplotte lijn vinden met de TI-84 Plus Silver Edition Welk element is altijd aanwezig in sulfiden?
Welk element is altijd aanwezig in sulfiden?  Wat zijn enkele redenen waarom mensen in een park de ene plant boven de andere zouden verkiezen?
Wat zijn enkele redenen waarom mensen in een park de ene plant boven de andere zouden verkiezen?  Waarom een computer niet het eerste is dat je nodig hebt als je kinderen leert coderen
Waarom een computer niet het eerste is dat je nodig hebt als je kinderen leert coderen een nieuwe, snellere manier om diblock-polymeermaterialen te verwerken
een nieuwe, snellere manier om diblock-polymeermaterialen te verwerken Een flitsende gele keelzanger? Daar zijn genen voor
Een flitsende gele keelzanger? Daar zijn genen voor Waarom zijn panda's met uitsterven bedreigde dieren?
Waarom zijn panda's met uitsterven bedreigde dieren?  Team combineert geavanceerde modellering met 300 jaar oude statistische analysetechniek om materiaaleigenschappen te verbeteren
Team combineert geavanceerde modellering met 300 jaar oude statistische analysetechniek om materiaaleigenschappen te verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


