
Wetenschap
Waarom zijn niet-polaire verbindingen onoplosbaar in water?
Niet-polaire verbindingen zijn daarentegen moleculen die geen polaire structuur hebben. Ze hebben geen positief of negatief uiteinde, dus ze worden niet aangetrokken door watermoleculen. Dit gebrek aan aantrekkingskracht betekent dat niet-polaire verbindingen niet in water oplossen.
Een voorbeeld van een niet-polaire verbinding is olie. Olie is een mengsel van koolwaterstoffen, dit zijn moleculen die zijn samengesteld uit koolstof- en waterstofatomen. Koolstof- en waterstofatomen zijn beide niet-polair, dus olie lost niet op in water.
Het onvermogen van niet-polaire verbindingen om in water op te lossen is om een aantal redenen belangrijk. Eén reden is dat we hierdoor niet-polaire verbindingen uit water kunnen scheiden met behulp van een proces dat extractie wordt genoemd. Extractie is een proces waarbij een oplosmiddel wordt gebruikt om een verbinding op te lossen die niet oplosbaar is in water. Het oplosmiddel wordt vervolgens van het water gescheiden en de verbinding wordt teruggewonnen.
Een andere reden waarom het onvermogen van niet-polaire verbindingen om in water op te lossen belangrijk is, is dat het helpt de structuur van levende wezens in stand te houden. De celmembranen van levende wezens bestaan uit een dubbellaag van fosfolipiden, een dubbele laag van fosfolipiden. Fosfolipiden zijn moleculen met een polaire kop en een niet-polaire staart. De polaire koppen van de fosfolipiden zijn naar buiten gericht, waar ze in wisselwerking staan met water, en de niet-polaire staarten zijn naar binnen gericht, waar ze met elkaar in wisselwerking staan. Deze opstelling creëert een barrière die voorkomt dat wateroplosbare moleculen de cel binnendringen en dat wateronoplosbare moleculen de cel verlaten.
 Als we een man op de maan kunnen zetten, we kunnen het Great Barrier Reef redden
Als we een man op de maan kunnen zetten, we kunnen het Great Barrier Reef redden Herkomst en soort:illegale houtkap bestrijden met wetenschap
Herkomst en soort:illegale houtkap bestrijden met wetenschap Wetenschappers creëren een nieuw idee over hoe je een opwarmende planeet kunt hacken:het drogen van de bovenste atmosfeer
Wetenschappers creëren een nieuw idee over hoe je een opwarmende planeet kunt hacken:het drogen van de bovenste atmosfeer  Onderschatting van geïrrigeerde gewassen leidt tot watertekorten
Onderschatting van geïrrigeerde gewassen leidt tot watertekorten Waarom hebben planten fotosynthese en cellulaire ademhaling nodig?
Waarom hebben planten fotosynthese en cellulaire ademhaling nodig?
Hoofdlijnen
- Iets om op te kauwen:Onderzoekers zoeken naar verbanden in de manier waarop dieren voedsel eten en verteren
- Hoe agro-ecologie onderdeel kan zijn van een ‘rechtvaardige transitie’ voor het Canadese voedselsysteem
- Vrouwelijke makaak in Italiaans heiligdom heeft haar gemummificeerde dode baby opgegeten
- In het ei leren Amerikaanse brulkikkers hoe ze kunnen voorkomen dat ze een lunch worden
- Top tien feiten over de menselijke blaas
- Wat moet ik doen als ik een eenzame, gezellige walvisachtigen tegenkom?
- Afrikaanse slaapziekte:hoe de ziekteverwekker tseetseevliegen koloniseert
- Producten vervaardigd door Anaerobe Ademhaling
- Anti-verouderingsbehandelingen - de wetenschap van het leven langer
- Nieuwe generatie kooldioxidegasscheidingssysteem met adsorbentia van het gate-type

- Chemici ontdekken een nieuw vormingsmechanisme van stoffen tegen kanker
- Een milieuvriendelijkere airconditioner

- Vloeibare metalen breken organische brandstoffen af tot ultradunne grafietplaten
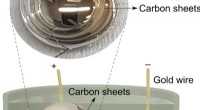
- Bacteriële hechting in vitro en in silico
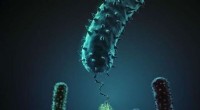
 Wetenschappers kunnen nu elektriciteit produceren uit tranen
Wetenschappers kunnen nu elektriciteit produceren uit tranen Doorbraak voor lab-on-a-chip materiaal
Doorbraak voor lab-on-a-chip materiaal Belangrijke innovatie op het gebied van fotonische componenten zou de supercomputertechnologie kunnen transformeren
Belangrijke innovatie op het gebied van fotonische componenten zou de supercomputertechnologie kunnen transformeren  Wat is antizwaartekracht?
Wat is antizwaartekracht?  Zet er maar op in:winsten in het ene type kracht geproduceerd door fusieverstoringen worden gecompenseerd door verliezen in een ander
Zet er maar op in:winsten in het ene type kracht geproduceerd door fusieverstoringen worden gecompenseerd door verliezen in een ander Qubit in een kristalrooster van boornitride is een geschikte sensor
Qubit in een kristalrooster van boornitride is een geschikte sensor Droogte boven zuidwestelijk Tibetaans plateau veroorzaakt door opwarming van de oceaan met meer dan 10, 000 mijl afstand
Droogte boven zuidwestelijk Tibetaans plateau veroorzaakt door opwarming van de oceaan met meer dan 10, 000 mijl afstand Technologie maakt steden slim, maar het kost ook het milieu
Technologie maakt steden slim, maar het kost ook het milieu
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

