
Wetenschap
Wat is het verschil tussen silicium en germanium volgens de atomaire structuur?
- Silicium (Si):Atoomnummer 14
- Germanium (Ge):Atoomnummer 32
Aantal protonen en elektronen:
- Silicium:14 protonen en 14 elektronen
- Germanium:32 protonen en 32 elektronen
Aantal neutronen:
- Silicium:14 neutronen (meest voorkomende isotoop, Si-28)
- Germanium:42 neutronen (meest voorkomende isotoop, Ge-74)
Elektronenconfiguratie:
- Silicium:2, 8, 4
- Germanium:2, 8, 18, 4
Atoomstraal:
- Silicium:111 picometer (pm)
- Germanium:122 uur
Ionische straal:
- Silicium:41 uur (Si4+)
- Germanium:17.00 uur (Ge4+)
Covalente straal:
- Silicium:237 uur
- Germanium:122 uur
Elektronegativiteit:
- Silicium:1,90 (Pauling-schaal)
- Germanium:2,01 (Pauling-schaal)
Kristalstructuur:
- Silicium:diamanten kubieke structuur
- Germanium:kubusvormige diamantstructuur (vergelijkbaar met silicium, maar met grotere roosterafstanden)
Bandafstand:
- Silicium:1,12 elektronvolt (eV) (bij kamertemperatuur)
- Germanium:0,67 eV (bij kamertemperatuur)
Mobiliteit van ladingdragers:
- Silicium:hogere mobiliteit van elektronen en gaten vergeleken met germanium
- Germanium:Lagere mobiliteit van elektronen en gaten vergeleken met silicium
Toepassingen:
- Silicium:wordt veel gebruikt in geïntegreerde schakelingen (IC's), transistors, zonnecellen en diverse elektronische apparaten vanwege de uitstekende halfgeleidende eigenschappen.
- Germanium:voornamelijk gebruikt in snelle elektronische apparaten, infraroodoptiek, stralingsdetectoren en enkele gespecialiseerde halfgeleiders.
 Stijgende zeeën aangewakkerd door klimaatverandering om in slechts 30 jaar $ 34 miljard aan onroerend goed in de VS te overspoelen, blijkt uit analyse
Stijgende zeeën aangewakkerd door klimaatverandering om in slechts 30 jaar $ 34 miljard aan onroerend goed in de VS te overspoelen, blijkt uit analyse Noordoost-VS graaft zich uit van niet-helemaal record sneeuwstorm
Noordoost-VS graaft zich uit van niet-helemaal record sneeuwstorm Onderzoekers voegen virtuele ruimtelijke verplaatsing toe aan extreme overstromingsscenario’s
Onderzoekers voegen virtuele ruimtelijke verplaatsing toe aan extreme overstromingsscenario’s  Klimaatverandering maakt zomerweer stormachtiger en toch meer stagnerend
Klimaatverandering maakt zomerweer stormachtiger en toch meer stagnerend Het is officieel:VK brak temperatuurrecord tijdens hittegolf
Het is officieel:VK brak temperatuurrecord tijdens hittegolf
Hoofdlijnen
- Wat zijn symbiotische relaties?
- Welke organismen kunnen het fotosyntheseproces uitvoeren?
- Waarom motten efficiëntere bestuivers kunnen zijn dan bijen en vlinders
- Hoe cellulaire machines eiwitten labelen voor afbraak
- Hoe Beschrijf de drie stappen in mendelstudies van erwtenplanten?
- Hoe antibioticaresistente microben zichzelf beschermen tegen aanvallen van lichaamsafweer
- Branden vuurspuwende draken hun tanden?
- Bonobo's en chimpansees:wat onze naaste familieleden ons over mensen vertellen
- Het AIM-algoritme verbetert microscoopbeelden met superresolutie in realtime
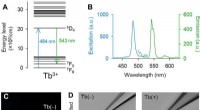
- Met terbium (III) gedoteerd fluorescerend glas voor biomedisch onderzoek
- Katalysator maakt reacties mogelijk met behulp van groen licht

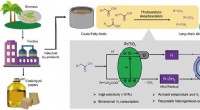
- Wetenschappers gebruiken licht om vetzuren om te zetten in alkanen
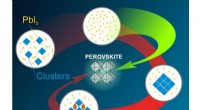
- Chemici bepalen hoe bijproducten bij de synthese van perovskieten kunnen worden vermeden
- Infraroodsensor dient als een nieuw hulpmiddel voor het ontdekken van medicijnen

 Oplaadstations voor elektrische auto's kunnen portalen zijn voor cyberaanvallen op het elektriciteitsnet
Oplaadstations voor elektrische auto's kunnen portalen zijn voor cyberaanvallen op het elektriciteitsnet Ideeën voor een Math Field Trip
Ideeën voor een Math Field Trip  Nieuw onderzoek beschrijft hoe uitgehongerde cellen eiwittransportstations kapen
Nieuw onderzoek beschrijft hoe uitgehongerde cellen eiwittransportstations kapen  Is lycopeen een polaire of niet-substantie?
Is lycopeen een polaire of niet-substantie?  Wijdverbreide maskering moedigt anderen aan om maskers te dragen
Wijdverbreide maskering moedigt anderen aan om maskers te dragen Het hijab-effect:feministische reactie op moslimimmigranten in Duitsland
Het hijab-effect:feministische reactie op moslimimmigranten in Duitsland De resultaten van een student-t-toets interpreteren
De resultaten van een student-t-toets interpreteren Oude botten onthullen twee walvissoorten die verloren zijn gegaan uit de Middellandse Zee
Oude botten onthullen twee walvissoorten die verloren zijn gegaan uit de Middellandse Zee
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

