
Wetenschap
Hoe maak je uit 37 procent HCL 0,5M HCL?
Stap 1:Bepaal de molariteit van de geconcentreerde HCl-oplossing.
De concentratie van de geconcentreerde HCl-oplossing wordt gegeven als 37% HCl. Dit betekent dat er 37 g HCl aanwezig is in 100 g van de oplossing. De molaire massa van HCl is 36,46 g/mol. Daarom kan de molariteit van de geconcentreerde HCl-oplossing als volgt worden berekend:
Molariteit (M) =(massa van HCl in gram) / (molaire massa van HCl in g/mol) x (volume van de oplossing in liters)
Molariteit (M) =(37 g) / (36,46 g/mol) x (100 ml / 1000 ml)
=10,13 M
Stap 2:Bereken het benodigde volume geconcentreerde HCl.
Om 0,5 M HCl te bereiden, moet u de geconcentreerde HCl-oplossing verdunnen met water. Het benodigde volume geconcentreerde HCl kan worden berekend met behulp van de formule:
Volume geconcentreerde HCl (ml) =(Gewenst volume oplossing in liters) x (Gewenste molariteit) / (Molariteit van geconcentreerde HCl)
Volume geconcentreerde HCl (ml) =(1 L) x (0,5 M) / (10,13 M)
=0,049 l of 49,4 ml
Stap 3:Bereid de 0,5 M HCl-oplossing voor.
Voeg in een zuurkast langzaam het berekende volume geconcentreerde HCl toe aan een container met gedestilleerd water. Wees voorzichtig bij het hanteren van geconcentreerde HCl, aangezien dit bijtend is. Voeg altijd zuur toe aan water, nooit water aan zuur. Roer de oplossing grondig om een uniforme menging te garanderen.
Stap 4:Pas het volume aan naar 1 liter.
Voeg extra gedestilleerd water toe aan de oplossing totdat het eindvolume 1 liter bedraagt. Meng goed om volledige homogeniteit te garanderen.
Door deze stappen te volgen, kunt u met succes 0,5 M HCl bereiden uit 37% HCl. Denk er altijd aan om de juiste persoonlijke beschermingsmiddelen (PBM) te dragen tijdens het werken met geconcentreerde zuren.
 Wetenschappers ontdekken hoe paardenkruid herbiciden van zich afschudt
Wetenschappers ontdekken hoe paardenkruid herbiciden van zich afschudt  Wat is de volledige ionische vergelijking voor H2SO4(aq) plus Cal2(aq) tot CaSO4(s) 2Hl(aq)?
Wat is de volledige ionische vergelijking voor H2SO4(aq) plus Cal2(aq) tot CaSO4(s) 2Hl(aq)?  Begrijpen hoe de monomeersequentie de geleiding in 'moleculaire draden' beïnvloedt
Begrijpen hoe de monomeersequentie de geleiding in 'moleculaire draden' beïnvloedt  Onderzoeker gebruikt canola om biologisch afbreekbare huishoudfolie te maken
Onderzoeker gebruikt canola om biologisch afbreekbare huishoudfolie te maken Superresolutiemicroscopie:nog dichter bij de limiet komen
Superresolutiemicroscopie:nog dichter bij de limiet komen
 Amerikaanse en Canadese wetenschappers gaan grensoverschrijdende overstromingen bestuderen
Amerikaanse en Canadese wetenschappers gaan grensoverschrijdende overstromingen bestuderen Studie:vernietiging door zeespiegelstijging in Californië kan groter zijn dan de ergste bosbranden en aardbevingen
Studie:vernietiging door zeespiegelstijging in Californië kan groter zijn dan de ergste bosbranden en aardbevingen Hardhandig optreden tegen evacuatie bevolen terwijl Filippijnse vulkaan oplaadt
Hardhandig optreden tegen evacuatie bevolen terwijl Filippijnse vulkaan oplaadt Plastic tassen kunnen milieuvriendelijker zijn dan papieren en katoenen tassen in steden als Singapore
Plastic tassen kunnen milieuvriendelijker zijn dan papieren en katoenen tassen in steden als Singapore Ideeën voor Controlled Variable Science Projects
Ideeën voor Controlled Variable Science Projects
Hoofdlijnen
- Eerste levensvormen op aarde onthuld in hete lente
- Onderzoek naar het genoom van inktvissen en octopussen laat zien hoe de unieke eigenschappen van koppotigen evolueerden
- Wat is homeiose?
- Parasieten van huisdieren die dieren in het wild wereldwijd aantasten
- Welke moleculen leveren energie voor spiercontracties?
- Kan een kunstmatig koraalrif de mariene biodiversiteit beschermen tegen klimaatveranderingen?
- Wetenschappers ontrafelen genetisch mysterie:waarom koralen levensreddende algen afwijzen
- Genetisch gemodificeerde gist levert intense hoparoma's op in bier, blijkt uit onderzoek
- Denken dieren rationeel? Onderzoeker suggereert dat rationele besluitvorming geen taal vereist
- Kunstmatige enzymfuncties evenals natuurlijke versie
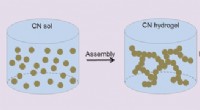
- Carbonitride-aerogels bemiddelen de fotokatalytische omzetting van water
- Molecuuleigenschappen veranderen door licht

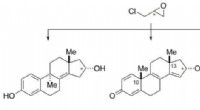
- Chemici stellen een nieuwe benadering voor van de synthese van het ABCD-ringsysteem van alpkinidine

- Onderzoekers ontwikkelen baanbrekend proces om kankerverwekkende medicijnen te maken
 Hoe het de Groenlandse ijskap verging in 2018
Hoe het de Groenlandse ijskap verging in 2018 Een lijst met weekdieren
Een lijst met weekdieren  Waarom stromen sommige vaste stoffen?
Waarom stromen sommige vaste stoffen?  Opslagcapaciteit voor cd's en microchips 100-voudig vergroten
Opslagcapaciteit voor cd's en microchips 100-voudig vergroten Welk doel dienen teken in het ecosysteem?
Welk doel dienen teken in het ecosysteem?  Expositie maakt virtuele interviews met overlevenden van de Holocaust mogelijk
Expositie maakt virtuele interviews met overlevenden van de Holocaust mogelijk Sterke aardbeving treft eilandketen voor Nieuw-Zeeland; geen tsunami
Sterke aardbeving treft eilandketen voor Nieuw-Zeeland; geen tsunami Visschubben kunnen draagbare elektronica duurzamer maken
Visschubben kunnen draagbare elektronica duurzamer maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

