
Wetenschap
Cumeen is een verbinding die alleen koolstof en waterstof bevat en die wordt gebruikt bij de productie van aceton, fenol, chemische industrie. Verbranding 47,6 mg cumeen produceert wat CO2 42,8 water?
We kunnen beginnen met het bepalen van het aantal mol koolstof en waterstof in de gegeven massa cumeen (47,6 mg).
Stap 1:Bereken het aantal mol CO2 en H2O
Uit de verbrandingsreactie weten we dat 47,6 mg cumeen 42,8 mg water produceert.
De molaire massa van CO2 is 44,01 g/mol en de molaire massa van H2O is 18,02 g/mol.
Aantal mol CO2 =(42,8 mg) / (44,01 g/mol) =0,000972 mol
Aantal mol H2O =(47,6 mg) / (18,02 g/mol) =0,00264 mol
Stap 2:Bepaal de mollen van C en H
Omdat elk molecuul CO2 één koolstofatoom bevat, is het aantal mol koolstof gelijk aan het aantal mol CO2.
Mol C =Aantal mol CO2 =0,000972 mol
Elk molecuul H2O bevat twee waterstofatomen, dus het aantal mol waterstof is tweemaal het aantal mol H2O.
Mol H =2 x Aantal mol H2O =2 x 0,00264 mol =0,00528 mol
Stap 3:Vind de eenvoudigste gehele getalsverhouding
Om de eenvoudigste gehele getalsverhouding te vinden, moeten we zowel het aantal koolstof- als waterstofmol delen door het kleinste aantal mol. In dit geval is het kleinste aantal mol 0,000972 mol (mol koolstof).
Mol C / 0,000972 mol =0,000972 / 0,000972 =1
Mol H / 0,000972 mol =0,00528 / 0,000972 =5,5
Stap 4:Schrijf de empirische formule
De empirische formule wordt geschreven met behulp van de gehele getalsverhouding verkregen in stap 3.
C:H =1:5,5
Omdat empirische formules altijd in de eenvoudigste verhouding van gehele getallen worden geschreven, moeten we de verhouding met 2 vermenigvuldigen om de meest eenvoudige formule te verkrijgen.
C:H =2:11
Daarom is de empirische formule voor cumeen C2H11.
Hoofdlijnen
- Waarom de toekomst van de landbouw vrouwelijk is
- Er is een organisme gevonden dat de volgende eigenschappen heeft. Is afhankelijk van planten voor voedingsstoffen. Wordt opgenomen via filamenten. Leeft in een vochtige omgeving. In welk koninkrijk hoort dit waarschijnlijk thuis?
- Wat termieten en cellen gemeen hebben
- Het fruitvliegmodel identificeert de belangrijkste toezichthouders achter de orgaanontwikkeling
- Het Trojan-Horse-mechanisme:hoe netwerken gendersegregatie verminderen
- Zebravissen laten zien hoe bio-elektriciteit de spierontwikkeling beïnvloedt
- Wat is het Atacama-skelet en waarom is het zo controversieel?
- Wat is de term voor wortel van een embryo?
- Een gezondheidscentrum voor jonge zalm
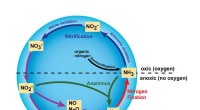
- De fijne kneepjes van de stikstofcyclus onderzoeken
- 'S Werelds beste gouden exemplaar onderzocht met Los Alamos-neutronen

- Machine learning maakt een optimaal ontwerp van anti-biofouling polymere borstelfilms mogelijk

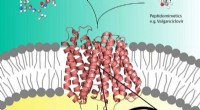
- Röntgenfoto's onthullen lay-out van geladen drugstransporter
- Het geheim van de Stradivari-viool bevestigd

 Elektronische activiteit die voorheen onzichtbaar was voor elektronenmicroscopen onthuld
Elektronische activiteit die voorheen onzichtbaar was voor elektronenmicroscopen onthuld China voert klimaatstrijd op met emissiehandelssysteem
China voert klimaatstrijd op met emissiehandelssysteem Bij Big Blue, Amerika's eerste zwarte software-engineer baande een pad maar betaalde een hoge prijs
Bij Big Blue, Amerika's eerste zwarte software-engineer baande een pad maar betaalde een hoge prijs Ultrakoude bubbels op ruimtestation openen nieuwe wegen voor kwantumonderzoek
Ultrakoude bubbels op ruimtestation openen nieuwe wegen voor kwantumonderzoek Synthetische robijnen maken
Synthetische robijnen maken Hoe wordt Photochemical Smog gevormd?
Hoe wordt Photochemical Smog gevormd?  Terug naar (nucleïsche) basen - DNA bestuderen aan boord van het internationale ruimtestation ISS
Terug naar (nucleïsche) basen - DNA bestuderen aan boord van het internationale ruimtestation ISS Diepgaande algoritmen helpen ruimteafval uit onze lucht te verwijderen
Diepgaande algoritmen helpen ruimteafval uit onze lucht te verwijderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


