
Wetenschap
Vergelijk de stabiliteit van een ammoniakcomplex versus een ethyleendiamine met een metaalion met coördinatiegetal 6 dat hoogstwaarschijnlijk zou reageren met een natriumhydroxideoplossing?
Over het algemeen zijn ethyleendiaminecomplexen voor een metaalion met een coördinatiegetal van 6 stabieler dan ammoniakcomplexen. Dit komt omdat ethyleendiamine een bidentaat ligand is, wat betekent dat het twee elektronenparen aan het metaalion kan doneren, terwijl ammoniak een monodentaat ligand is en slechts één elektronenpaar kan doneren. Het chelaateffect, dat verwijst naar de verhoogde stabiliteit van een complex met een multidentaatligand vergeleken met een complex met meerdere monodentaatliganden, draagt bij aan de verbeterde stabiliteit van ethyleendiaminecomplexen.
Bij het beschouwen van de reactie van deze complexen met natriumhydroxide-oplossing speelt de basiciteit van de liganden ook een rol. Ammoniak is een zwakkere base dan ethyleendiamine, wat betekent dat het minder waarschijnlijk is dat het protoneert in een waterige oplossing. Als gevolg hiervan is het waarschijnlijker dat ammoniakcomplexen liganduitwisselingsreacties ondergaan met hydroxide-ionen uit natriumhydroxideoplossing, wat leidt tot de vorming van metaalhydroxidecomplexen.
Daarentegen is ethyleendiamine een sterkere base en is het minder waarschijnlijk dat de complexen liganduitwisselingsreacties met hydroxide-ionen ondergaan. Daarom zijn ethyleendiaminecomplexen over het algemeen stabieler in aanwezigheid van natriumhydroxideoplossing vergeleken met ammoniakcomplexen.
 Een bosgloed onthult ontwaken uit de winterslaap
Een bosgloed onthult ontwaken uit de winterslaap Wat is stormvloed? Het is vaak de dodelijkste en meest destructieve dreiging van orkanen
Wat is stormvloed? Het is vaak de dodelijkste en meest destructieve dreiging van orkanen Oekraïne opent gigantische koepel boven verwoeste reactor van Tsjernobyl
Oekraïne opent gigantische koepel boven verwoeste reactor van Tsjernobyl Hoe gymnasten te beschermen tegen gevaarlijke chemicaliën in sportschoolfaciliteiten?
Hoe gymnasten te beschermen tegen gevaarlijke chemicaliën in sportschoolfaciliteiten? Waar denk je aan? Facebook zegt dat naaktbeelden dat niet mogen zijn
Waar denk je aan? Facebook zegt dat naaktbeelden dat niet mogen zijn
Hoofdlijnen
- Hoe een 'dirigent' betekenis geeft aan chaos in vroege muizenembryo's
- Studie:Lagunes van de vergeten kust van de Noordpool kwetsbaar voor klimaatverandering en menselijke ontwikkeling
- Welke ziekten hebben een kleine vitale capaciteit?
- Wat zijn de twee systemen die lichaamsfuncties controleren?
- Wat zijn anaerobe infecties?
- Onderzoekers ontwikkelen een systeem om te beoordelen hoe effectief soorten zijn bij het bestuiven van gewassen
- Hoe wordt het lichaamsframe genoemd?
- Een fokprogramma voor natuurbehoud opzetten om de laatste saola te redden
- De oorsprong van het leven ontrafelen:vijf belangrijke doorbraken van de afgelopen vijf jaar
- Wetenschappers ontdekken pad naar verbetering van baanbrekende batterij-elektrode

- Proces zet polyethyleen zakken, plastics om in polymere bouwstenen
- Een nieuwe manier om zachte robots te maken:DNA-triggers die ervoor zorgen dat hydrogels van vorm veranderen

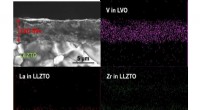
- Kathodefabricage voor oxide solid-state batterijen bij kamertemperatuur
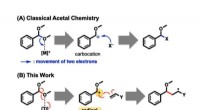
- Radicale chemie maakt eenvoudige synthese van ethers mogelijk
 Geef houtkachels de schuld van luchtvervuiling en gezondheidsbedreigingen in de winter
Geef houtkachels de schuld van luchtvervuiling en gezondheidsbedreigingen in de winter Om creativiteit aan te wakkeren, ideeën uitwerken en dan weggaan
Om creativiteit aan te wakkeren, ideeën uitwerken en dan weggaan Miljoenen microdeeltjes in een oogwenk microprinten via multi-foton 3D-laserprinten
Miljoenen microdeeltjes in een oogwenk microprinten via multi-foton 3D-laserprinten  Hoe lang duurt het om een archeologische opgravingslocatie op te graven?
Hoe lang duurt het om een archeologische opgravingslocatie op te graven?  De voordelen van het hebben van een groot aantal chromosomen
De voordelen van het hebben van een groot aantal chromosomen Onderzoekers observeren dynamische kwantumfase-overgangen in een interactief veellichamensysteem
Onderzoekers observeren dynamische kwantumfase-overgangen in een interactief veellichamensysteem UITLEGGER:Wat is een derecho?
UITLEGGER:Wat is een derecho?  Op de rebound
Op de rebound
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

