
Wetenschap
Wat gebeurt er als magnesium reageert met verdund zwavelzuur?
Mg(s) + H2SO4(aq) → MgSO4(aq) + H2(g)
In deze reactie:
- Magnesium (Mg) in zijn vaste vorm(en) is het reagerende metaal.
- Verdund zwavelzuur (H2SO4), een waterige oplossing, is het reactantzuur.
De reactie omvat een enkele verdringings- of substitutiereactie. Dit is wat er gebeurt:
1. Magnesiumatomen (Mg) in vaste vorm verliezen hun twee buitenste elektronen en worden elk Mg2+-ionen.
2. De verloren elektronen van magnesiumatomen worden overgebracht naar waterstofionen (H+) in de zwavelzuuroplossing, waardoor ze worden gereduceerd tot waterstofgas (H2).
3. De positief geladen Mg2+-ionen combineren met de negatief geladen sulfaationen (SO42-) uit zwavelzuur en vormen magnesiumsulfaat (MgSO4), dat oplost in de oplossing.
Als gevolg hiervan wordt magnesiumsulfaat (MgSO4), een oplosbaar zout, gevormd en komt waterstofgas (H2) als bijproduct vrij. Deze reactie wordt vaak waargenomen tijdens laboratoriumdemonstraties of experimenten waarbij de reactiviteit van metalen met zuren betrokken is.
Hoofdlijnen
- Ecologische successie: definitie, types, stadia en voorbeelden
- Hoe antidepressiva werken
- Wat gebruiken planten voor fotosynthese?
- Wetenschappers bepalen hoe regenboogforel op de juiste manier kan worden gevoerd
- Nieuwe 'atlas' biedt ongekende inzichten over hoe genen functioneren in de vroege embryo-ontwikkeling
- Genetische studie onthult evolutionaire geschiedenis van dingo's
- Kennis van larvale vissen slechts een druppel op de gloeiende plaat
- Kleine opgerolde eiwitrollen die zichzelf in kooien assembleren
- Niet alle dieren in het wild zijn hersteld in lockdowns, zo blijkt uit nieuw onderzoek
- Elektrochemie spoelt antibioticaresistente eiwitten weg

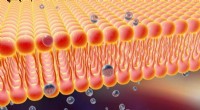
- Fluorescerende sondes bewijzen het bestaan van celmembraanstructuren van lipidenvlotten
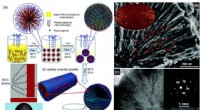
- Chemici ontwikkelen milieuvriendelijke nanocomposieten uit fruit- en bessenschillen

- Hiërarchisch mesoporeuze titaniumdioxidematerialen voor energie- en milieutoepassingen
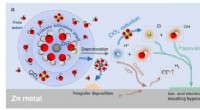
- Gehydrateerde eutectische elektrolyten helpen de prestaties van waterige zinkbatterijen te verbeteren
 Egg in Bottle Science Projects
Egg in Bottle Science Projects  GAMEOPT:een algoritme om de doorstroming van voertuigen door dynamische niet-gesignaleerde kruispunten te optimaliseren
GAMEOPT:een algoritme om de doorstroming van voertuigen door dynamische niet-gesignaleerde kruispunten te optimaliseren nanodeeltjes, van hype tot daadwerkelijk klinisch product
nanodeeltjes, van hype tot daadwerkelijk klinisch product 3D-scans van vleermuisschedels helpen natuurhistorische musea om donkere hoeken van hun collecties te openen
3D-scans van vleermuisschedels helpen natuurhistorische musea om donkere hoeken van hun collecties te openen Kijken in het hart van een supernova:Simulatie laat zien hoe je een snel draaiende stellaire kern kunt detecteren
Kijken in het hart van een supernova:Simulatie laat zien hoe je een snel draaiende stellaire kern kunt detecteren  Nieuwe ultradunne optische holtes maken gelijktijdige kleurproductie op een elektronische chip mogelijk
Nieuwe ultradunne optische holtes maken gelijktijdige kleurproductie op een elektronische chip mogelijk Onderzoekers ontdekken dat blootstelling aan nanodeeltjes de gezondheid van het hart kan bedreigen
Onderzoekers ontdekken dat blootstelling aan nanodeeltjes de gezondheid van het hart kan bedreigen Afbeelding:sporen van zomerschepen in de Stille Oceaan
Afbeelding:sporen van zomerschepen in de Stille Oceaan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


